Medicinsk ekspert af artiklen
Nye publikationer
Goodpastures syndrom: årsager, symptomer, diagnose, behandling
Sidst revideret: 12.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
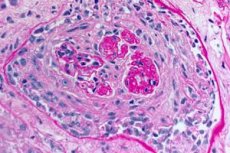
Goodpastures syndrom er et autoimmunt syndrom, der involverer alveolær lungeblødning og glomerulonefritis forårsaget af cirkulerende anti-GBM-antistoffer. Goodpastures syndrom udvikles oftest hos personer med en genetisk prædisposition, der ryger cigaretter, men kulbrinteinhalation og virale luftvejsinfektioner er mulige yderligere faktorer. Symptomer på Goodpastures syndrom omfatter dyspnø, hoste, træthed, hæmoptyse og/eller hæmaturi. Goodpastures syndrom mistænkes hos patienter med hæmoptyse eller hæmaturi og bekræftes af tilstedeværelsen af anti-GBM-antistoffer i blodet. Behandling af Goodpastures syndrom omfatter plasmaudskiftning, glukokortikoider og immunsuppressive midler såsom cyclophosphamid. Prognosen er god, hvis behandlingen påbegyndes, før respirations- eller nyresvigt udvikler sig.
Goodpastures syndrom blev først beskrevet af Goodpasture i 1919. Goodpastures syndrom er en kombination af glomerulonefritis og alveolær blødning i nærvær af anti-GBM-antistoffer. Goodpastures syndrom viser sig oftest som en kombination af diffus alveolær blødning og glomerulonefritis, men forårsager undertiden isoleret glomerulonefritis (10-20%) eller lungepåvirkning (10%). Mænd rammes oftere end kvinder.
Hvad forårsager Goodpasture syndrom?
Årsagen til sygdommen er ikke præcist fastslået. Der antages en genetisk prædisposition for Goodpastures syndrom, og dens markør anses for at være tilstedeværelsen af HLA-DRW2. Der er et synspunkt om den mulige rolle af en tidligere virusinfektion (hepatitis A-virus og andre virussygdomme), industrielle farer og medicin (primært D-penicillamin).
Grundlaget for patogenesen af Goodpastures syndrom er dannelsen af autoantistoffer mod basalmembranerne i glomerulære kapillærer i nyrerne og alveolerne. Disse antistoffer tilhører IgG-klassen, de binder sig til antistofferne i basalmembranerne i nærvær af komplementkomponenten C3 med den efterfølgende udvikling af immunbetændelse i nyrerne og lungealveolerne.
Anti-GBM-antistoffer er rettet mod det ikke-kollagene (NC-1) domæne af 3. kæden af type IV-kollagen, som findes i højeste koncentration i basalmembranerne i nyre- og pulmonale kapillærer. Eksponering for miljøfaktorer - rygning, virale ARI'er og inhalation af hydrocarbonatsuspensioner (oftere) - og sjældnere lungebetændelse aktiverer præsentationen af alveolære kapillære antigener til cirkulerende antistoffer hos personer med en arvelig prædisposition (oftest er disse bærere af HLA-DRwl5-, -DR4- og -DRB1-allelerne). Cirkulerende anti-GBM-antistoffer binder sig til basalmembraner, fikserer komplement og inducerer en cellulær inflammatorisk respons, hvilket fører til udvikling af glomerulonefritis og/eller pulmonal kapillaritis.
Der er sandsynligvis en vis fællesnævner for autoantigener i basalmembranen i nyrernes og alveolernes glomerulære kapillærer. Autoantigenet dannes under påvirkning af den skadelige effekt af den ætiologiske faktor. En ukendt ætiologisk faktor beskadiger og ændrer strukturen af basalmembranerne i nyrerne og lungerne. Udskillelsen af de resulterende nedbrydningsprodukter fra nyrernes glomerulære basalmembraner aftager og mindskes, når de beskadiges, hvilket naturligt skaber forudsætningerne for udvikling af autoimmune skader på nyrer og lunger. Det er stadig ikke fuldstændigt kendt, hvilken komponent af basalmembranen der bliver autoantigenet. I øjeblikket antages det, at dette er den interne strukturelle komponent i nyrernes glomerulære basalmembran, a3-kæden af type 4 kollagen.
De dannede immunkomplekser aflejres langs basalmembranerne i de glomerulære kapillærer, hvilket fører til udviklingen af en immuninflammatorisk proces i renal glomerulus (glomerulonefritis) og alveolerne (alveolitis). De vigtigste celler, der er involveret i udviklingen af denne immuninflammation, er T-lymfocytter, monocytter, endotelocytter, polymorfonukleære leukocytter og alveolære makrofager. Interaktionen mellem dem sikres af molekylære mediatorer, cytokiner (vækstfaktorer - blodplader, insulinlignende, b-transformerende; interleukin-1, tumornekrosefaktor osv.). Arachidonsyremetabolitter, frie iltradikaler, proteolytiske enzymer og adhæsive molekyler spiller en vigtig rolle i udviklingen af immuninflammation.
Aktivering af alveolære makrofager er af stor betydning i udviklingen af alveolitis ved Goodpastures syndrom. I aktiveret tilstand udskiller de omkring 40 cytokiner. Gruppe I-cytokiner (kemotaxiner, leukotriener, interleukin-8) forbedrer strømmen af polymorfonukleære leukocytter ind i lungerne. Gruppe II-cytokiner (vækstfaktorer - blodplader, makrofager) fremmer bevægelsen af fibroblaster ind i lungerne. Alveolære makrofager producerer også aktive former for ilt, proteaser, som beskadiger lungevævet.
Patomorfologi af Goodpastures syndrom
De vigtigste patomorfologiske manifestationer af Goodpastures syndrom er:
- overvejende skade på mikrocirkulationslejet i nyrer og lunger. I lungerne observeres et billede af venulitis, arteriolitis, kapillaritis med udtalte fænomener af destruktion og proliferation; skade på kapillærerne observeres hovedsageligt i de interalveolære septa, alveolitis med hæmoragisk ekssudat i alveolerne udvikler sig. Nyreskade er karakteriseret ved udvikling af ekstrakapillær proliferativ glomerulonefritis med efterfølgende dannelse af hyalinose og fibrose, hvilket fører til udvikling af nyresvigt;
- udtalte intraalveolære blødninger;
- udvikling af pulmonal hæmosiderose og pneumosklerose af varierende sværhedsgrad som følge af udviklingen af alveolitis.
Symptomer på Goodpastures syndrom
Sygdommen præsenterer sig oftest med kliniske manifestationer af lungepatologi. Hæmoptyse er det mest fremtrædende symptom; hæmoptyse kan dog være fraværende i nærvær af hæmoragiske manifestationer, og patienten kan kun præsentere med infiltrative forandringer på røntgenbillede af thorax eller med et infiltrat og respirationsbesvær og/eller -svigt. Dyspnø (primært ved anstrengelse), hoste, utilpashed, nedsat arbejdsevne, brystsmerter, feber og vægttab er almindelige. Op til 40 % af patienterne har makrohæmaturi, selvom lungeblødning kan gå forud for nyremanifestationer med uger til år.
Under hæmoptyse kan åndenøden tiltage. Svaghed og nedsat arbejdsevne er også en bekymring.
Symptomerne på Goodpastures syndrom varierer over tid og spænder fra klare lunger ved auskultation til knitrende og tørre raslen. Nogle patienter har perifert ødem og bleghed på grund af anæmi.
Under undersøgelsen rettes opmærksomheden mod bleg hud, cyanose af slimhinderne, pastøsitet eller udtalt hævelse i ansigtet, nedsat muskelstyrke og vægttab. Kropstemperaturen er normalt forhøjet til feberniveau.
Ved perkussion af lungerne kan en forkortelse af perkussionslyden konstateres over omfattende foci af lungeblødning, men dette observeres sjældent; oftere er der ingen ændringer i perkussionslyden.
Et karakteristisk auskultatorisk tegn på Goodpastures syndrom er tør og våd hvæsen, hvis antal stiger betydeligt under eller efter hæmoptyse.
Ved undersøgelse af det kardiovaskulære system afsløres arteriel hypertension, muligvis en stigning i grænsen for relativ hjertesløvhed til venstre, dæmpede hjertelyde, en blød systolisk mumlen og perikardiel friktionsmumlen opstår med udviklingen af alvorlig nyresvigt. Ved progressiv nyreskade på baggrund af betydelig arteriel hypertension kan akut venstre ventrikel svigt med et billede af hjerteastma og lungeødem udvikle sig. Normalt udvikler denne situation sig i sygdommens terminale stadium.
Som regel manifesterer nyreskade sig senere, efter en vis tid efter udviklingen af lungesymptomer. Karakteristiske kliniske tegn på nyrepatologi er hæmaturi (undertiden makrohæmaturi), hurtigt fremadskridende nyresvigt, oliguri, arteriel hypertension.
I 10-15% af tilfældene begynder Goodpastures syndrom med kliniske tegn på nyrepatologi - det kliniske billede af glomerulonefritis optræder (oliguri, ødem, arteriel hypertension, udtalt bleghed), og derefter deltager symptomer på lungeskade. Mange patienter kan have muskelsmerter, ledsmerter.
Uanset de forskellige debutvarianter er Goodpastures syndrom i de fleste tilfælde alvorligt, sygdommen udvikler sig støt, og der udvikles alvorlig lunge- og nyresvigt. Patienternes forventede levetid fra sygdommens debut varierer fra flere måneder til 1-3 år. Oftest dør patienterne af uræmi eller lungeblødning.
Hvad generer dig?
Diagnose af Goodpasture syndrom
Diagnosen Goodpastures syndrom kræver påvisning af serum-anti-GBM-antistoffer ved indirekte immunofluorescens eller, når det er muligt, ved direkte enzymbundet immunosorbentassay (ELISA) med rekombinant humant NC-1 α3. Andre serologiske tests, såsom antinukleære antistoffer (ANA)-test, anvendes til at påvise SLE, og antistreptolysin-O-titer bruges til at påvise poststreptokok glomerulonefritis, som kan være årsagen til mange tilfælde af pulmonalt-renalt syndrom. ANCA er positiv (i perifere prøver) i 25 % af tilfældene af Goodpastures syndrom. Nyrebiopsi kan være indiceret, hvis glomerulonefritis er til stede (hæmaturi, proteinuri, røde blodlegemerslam ved urinanalyse og/eller nyresvigt). Hurtigt progressiv fokal segmental nekrotiserende glomerulonefritis med et progressivt forløb findes ved biopsi ved Goodpastures syndrom og alle andre årsager til pulmonalt-renalt syndrom. Immunofluorescensfarvning af nyre- eller lungevæv afslører klassisk lineær aflejring af IgG langs glomerulære eller alveolære kapillærer. Det ses også ved diabetisk nyre og fibrillær glomerulonefritis, en sjælden lidelse, der forårsager pulmonalt-renalt syndrom, men påvisning af GBM-antistoffer ved disse lidelser er uspecifik.
Lungefunktionstest og bronkoalveolær lavage er ikke diagnostiske for Goodpastures syndrom, men kan bruges til at bekræfte tilstedeværelsen af diffus alveolær blødning hos patienter med glomerulonefritis og lungeinfiltrater, men uden hæmoptyse. Lavagevæske, der forbliver hæmoragisk efter flere skylninger, kan bekræfte diffust hæmoragisk syndrom, især hvis der er et samtidig fald i hæmatokrit.
 [ 3 ]
[ 3 ]
Laboratoriediagnostik af Goodpastures syndrom
- Generel blodprøve. Karakteristiske træk er jernmangelhypokrom anæmi, hypokromi, anisocytose, poikilocytose af erytrocytter. Leukocytose, venstreforskydning af leukocytformlen og en signifikant stigning i ESR observeres også.
- Generel urinanalyse. Protein (graden af proteinuri kan være betydelig), cylindre (granulær, hyaline, erytrocyt), erytrocytter (makrohæmaturi kan forekomme) findes i urinen. Efterhånden som kronisk nyresvigt udvikler sig, falder urinens relative tæthed, og isohyposthenuri udvikler sig i Zimnitsky-testen.
- Biokemisk blodprøve. Forhøjede blodniveauer af urinstof, kreatinin, haptoglobin, seromucoid, a2 og gammaglobuliner, nedsat jernindhold.
- Immunologiske undersøgelser. Et fald i antallet af T-lymfocytsuppressorer kan detekteres, cirkulerende immunkomplekser detekteres. Antistoffer mod basalmembranen i glomerulære og alveolære kapillærer detekteres ved indirekte immunofluorescens eller radioimmunologiske metoder.
- Sputumanalyse. Sputum indeholder mange erytrocytter, hæmosiderin og siderofager.
Instrumentel diagnostik af Goodpastures syndrom
- Røntgenundersøgelse af lungerne. Karakteristiske røntgentegn er lungeinfiltrater i rodregionen, der spreder sig til de nedre og midterste dele af lungerne, samt progressive, symmetriske, bilaterale skylignende infiltrater.
- Undersøgelse af den eksterne respirations funktion. Spirometri afslører en restriktiv type respirationssvigt (nedsat vitalkapacitet), og efterhånden som sygdommen skrider frem, tiltræder en obstruktiv type respirationssvigt (nedsat FEV1, Tiffeneau-indeks).
- EKG. Tegn på svær myokarddystrofi af anæmisk og hypoksisk oprindelse afsløres (reduktion i T-bølgernes amplitude og ST-intervallet i mange afledninger, oftest i venstre brystafledning). Ved svær arteriel hypertension optræder tegn på venstre ventrikels myokardhypertrofi.
- Blodgasanalyse afslører arteriel hypoxæmi.
- Undersøgelse af lunge- og nyrebiopsier. Hvis det er umuligt at stille en nøjagtig diagnose ved hjælp af ikke-invasive metoder, udføres en biopsi af lungevævet (åben biopsi) og nyrerne for endelig verifikation af diagnosen. Histologisk og immunologisk undersøgelse af biopsierne udføres. Følgende tegn er karakteristiske for Goodpastures syndrom:
- tilstedeværelsen af morfologiske tegn på glomerulonefritis (oftest ekstrakapillær), hæmoragisk alveolitis, hæmosiderose og interstitiel fibrose;
- detektion af lineære aflejringer af IgG og komplementkomponent C3 på basalmembranerne i pulmonalveolerne og renale glomeruli ved hjælp af immunofluorescensmetoden.
Diagnostiske kriterier for Goodpasture syndrom
Når man stiller diagnosen Goodpastures syndrom, anbefales det at bruge følgende kriterier.
- En kombination af lungepatologi og nyrepatologi, dvs. hæmoptyse (ofte lungeblødning), åndenød og symptomer på glomerulonefritis.
- Sygdommens forløb er støt progressivt med udvikling af respirations- og nyresvigt.
- Udvikling af jernmangelanæmi.
- Detektion under radiografisk undersøgelse af lungerne af flere bilaterale skylignende infiltrater på baggrund af retikulær deformation af lungemønsteret.
- Påvisning i blodet af høje titere af cirkulerende antistoffer mod basalmembranen i renale glomeruli og alveoler.
- Detektion af lineære aflejringer af IgG og komplementkomponent C3 på basalmembranerne i glomerulære og alveolære kapillærer.
- Fravær af andre systemiske (undtagen pulmonale og nyre) manifestationer.
Differentialdiagnose af Goodpasture syndrom
Goodpastures syndrom skal differentieres fra en række sygdomme, der manifesterer sig ved hæmoptyse eller lungeblødning. Det er nødvendigt at udelukke onkologiske sygdomme i bronkier og lunger, tuberkulose, lungeabcesser, bronkiektasi, hjerte- og karsygdomme (som fører til overbelastning og hypertension i lungekredsløbet), systemisk vaskulitis og hæmoragisk diatese.
Screeningsprogram for Goodpastures syndrom
- Generelle blod- og urinprøver.
- Biokemisk blodprøve: bestemmelse af totalt protein og proteinfraktioner, kreatinin og urinstof, transaminaser, seromucoid, haptoglobin, fibrin, jern.
- Sputumanalyse: cytologisk undersøgelse, bestemmelse af siderofager.
- Immunologiske undersøgelser: bestemmelse af indholdet af B- og T-lymfocytter, delpopulationer af T-lymfocytter, immunoglobuliner, cirkulerende immunkomplekser, antistoffer mod basalmembranerne i glomeruli i nyrerne og alveolerne.
- Røntgenundersøgelse af lungerne.
- EKG.
- Spirometri.
- Undersøgelse af lunge- og nyrebiopsier.
Hvilke tests er nødvendige?
Behandling af Goodpastures syndrom
Behandling af Goodpastures syndrom omfatter daglig eller hver anden dag plasmaudskiftning i 2 til 3 uger (4 L plasmaudskiftning) for at fjerne anti-GBM-antistoffer, kombineret med intravenøse glukokortikoider (normalt methylprednisolon 1 g over mindst 20 minutter hver anden dag 3 gange med prednisolon 1 mg/kg kropsvægt dagligt) og cyclophosphamid (2 mg/kg én gang dagligt) i 6 til 12 måneder for at forhindre dannelse af nye antistoffer. Terapien kan nedtrappes, når lunge- og nyrefunktionen ophører med at forbedres. Langtidsdødelighed er relateret til graden af nyresvigt ved sygdomsdebut; patienter, der kræver dialyse tidligt, og dem med mere end 50% halvmåneformede nefroner ved biopsi, har overlevelsestider på mindre end 2 år og kræver ofte dialyse, medmindre nyretransplantation overvejes. Hæmoptyse kan være et godt prognostisk tegn, fordi det fører til tidligere opdagelse af sygdommen; mindretallet af patienter, der er ANCA-positive, reagerer bedre på behandling af Goodpastures syndrom. Tilbagefald forekommer i en lille procentdel af tilfældene og er forbundet med fortsat rygning og luftvejsinfektion. Hos patienter med nyresygdom i slutstadiet, som har fået foretaget en nyretransplantation, kan sygdommen komme tilbage i transplantatet.
Hvad er prognosen for Goodpastures syndrom?
Goodpastures syndrom er ofte hurtigt progredierende og kan være fatalt, medmindre det diagnosticeres og behandles omgående; prognosen er god, når behandlingen påbegyndes, før respirations- eller nyresvigt udvikler sig.
Øjeblikkelig overlevelse ved lungeblødning og respirationssvigt er forbundet med at sikre luftvejenes passage; endotrakeal intubation og mekanisk ventilation anbefales til patienter med grænsetilfælde i arterielle blodgasser og truende respirationssvigt.

