Medicinsk ekspert af artiklen
Nye publikationer
Diagnose af stadier af prostatakræftforløb
Sidst revideret: 04.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Klinisk skelnes der mellem lokaliseret (T1-2 , N0 , M0 ), lokalt fremskreden (T3-4 , N0-1 , M0 ) og generaliseret kræft (T1-4 , N0-1 , M1 ).
Patienter med klinisk lokaliserede og lokalt avancerede stadier klassificeres efter risikograd (D'Amico A V. et al., 2003):
- lav: stadium T 1a-c; PSA-niveau mindre end 10 ig/ml: Gleason-gradering - 2-5; i biopsi - ensidig læsion mindre end 50%:
- moderat: stadium T 2a; PSA-niveau mindre end 10 ng/ml; Gleason-score - 3 + 4 = 7; i biopsi - bilateral læsion mindre end 50%;
- højt stadie T2b , T3a -b; PSA-niveau - 10-20 ng/ml; Gleason-gradering - mere end 4 + 3 - 7; i biopsi - skade mere end 50%, perineural invasion;
- meget højt: stadium T 4; PSA-niveau over 20 ng/ml; Gleason-score over 8; biopsi viser lymfovaskulær invasion.
Efter diagnosen er afklaret, og processens omfang er fastslået (lokaliseret, lokalt fremskreden eller generaliseret), står lægen og patienten over for et valg af behandlingsmetode. I det moderne samfund lægges der stor vægt på patienternes livskvalitet efter behandlingsstart. Livskvaliteten uden behandling svarer til forløbet af den underliggende sygdom og afhænger af progressionen af den onkologiske proces. Ændringer i livskvaliteten forekommer hovedsageligt efter behandlingsstart og brug af en af de terapeutiske eller kirurgiske metoder. En klar fastlæggelse af processens stadie gør det ikke kun muligt at vælge den optimale behandlingsmetode, men også at forudsige sygdommens videre forløb.
Bestemmelse af PSA-niveauet i kombination med det kliniske billede af prostatakræft og tumorens gradering i henhold til Gleason-skalaen øger informationsindholdet i hver af de anførte indikatorer betydeligt ved fastlæggelsen af kræftens patologiske stadium. AV Partin et al. (1997) foreslog prognostiske tabeller, der gør det muligt at forudsige tumorens videre spredning, valg af behandlingsmetode, graden af radikalitet og prognosen for behandlingens effektivitet.
For at vurdere tumorens spredning er de mest almindeligt anvendte metoder DRE, TRUS, bestemmelse af PSA-niveauet og knoglescintigrafi. Om nødvendigt ordineres computertomografi (CT) eller magnetisk resonansbilleddannelse (MRI) og røntgenbillede af thorax.
Enhver af billeddiagnostiske metoder er designet til at bestemme stadiet og vurdere behandlingens effektivitet. Efter at have verificeret diagnosen skal urologen afklare den primære tumors størrelse, dens grænser, tumorens invasive eller metastatiske potentiale. Alle disse indikatorer er af stor betydning for sygdommens prognose og valget af behandlingsmetode.
Primær tumor (T)
Først og fremmest er det nødvendigt at afgøre, om tumoren er begrænset til prostata (T 1-2 ) eller strækker sig ud over kapslen (T 3-4 ). Digital undersøgelse giver ofte ikke mulighed for at vurdere tumorens spredning. Ifølge nogle data svarer resultaterne af DRE til resultaterne af histologisk undersøgelse hos mindre end 50% af patienterne. En mere detaljeret undersøgelse er dog kun indiceret, når der træffes beslutning om radikal behandling.
PSA-niveauet kan afspejle tumorens omfang, men tillader ikke en nøjagtig bestemmelse af det morfologiske stadie. Kombinationen af PSA-niveau, Gleason-indeks og palpationsdata giver mulighed for en bedre forudsigelse af det morfologiske stadie end hver af disse parametre separat. Værdien af fri PSA er kontroversiel: i én undersøgelse hjalp bestemmelse af indholdet af fri PSA med at afklare stadiet i lokaliserede tumorer, men andre undersøgelser bekræftede ikke dette. Kun dybdegående undersøgelser vil hjælpe med at løse dette problem.
Transrektal ultralyd bruges oftest til at undersøge prostataens tilstand. Denne metode kan kun opdage 60% af tumorer og viser ikke altid kapselinvasion. Næsten 60% af patienterne har stadium T3 . Ultralyd indikerer en mindre almindelig proces. Ultralydstegn på kapselinvasion er udbuling, ujævnheder og ruptur af kirtelkonturen. Invasion af tumorceller i sædblærerne er et dårligt prognostisk tegn, men information om det er ekstremt vigtig for valg af en behandlingsmetode. Ved udførelse af TRUS skal man være opmærksom på vesiklernes ekkostruktur (hyperekogenicitet), deres asymmetri, deformation og ekspansion. Skade på sædblærerne indikeres også af tab af rundhed og kompaktering ved kirtelbunden. Disse tegn er ret subjektive, så det er uhensigtsmæssigt at stole udelukkende på ultralydsdata. Invasion af sædblærerne indikerer en høj risiko for lokalt tilbagefald og metastaser, og deres biopsi er indiceret til afklaring (før operation). Undersøgelsen bør ikke påbegyndes med denne procedure, men hvis risikoen for invasion er høj, og valget af behandling afhænger af biopsiresultatet, er implementeringen berettiget. Et negativt resultat udelukker ikke mikroskopisk invasion. Som regel udføres en biopsi af sædblærerne i det kliniske stadie T 2b og højere, og PSA-indholdet er mere end 10 ng/ml. Resultatet betragtes som positivt, hvis mindst én biopsi fra prostatabunden indeholder tumorceller. Ikke kun yderligere undersøgelser, men også en grundig analyse af resultaterne af den primære biopsi gør det muligt at øge nøjagtigheden af den kliniske bestemmelse af stadiet (antallet og omfanget af tumorfoci, kapselinvasion spiller en rolle). Graden af differentiering er også vigtig: med et Gleason-indeks på mindre end 6 er tumoren lokaliseret i 70% af tilfældene.
Blodgennemstrømningen i prostata ved kræft er højere end i en normal kirtel eller ved hyperplasi. Efter kastration reduceres intensiteten af blodgennemstrømningen i kirtlen. Udviklingen af ekkodopplerografiske kort til diagnose og overvågning af prostatakræft er lovende, men der findes i øjeblikket ingen pålidelige data om brugen af ekkodopplerografi til bestemmelse af stadiet i den lokale proces. Det er muligt at bruge denne metode til at opnå yderligere materiale under målrettet biopsi fra foci af patologisk vaskularisering.
Resultaterne af visualisering af prostatakræft afhænger direkte af klinikkens tekniske udstyr og specialistens erfaring. Derfor spiller alle moderne visualiseringsmetoder ikke en afgørende, men en afklarende rolle, og valget af behandlingsmetode er baseret på en kombination af kliniske undersøgelsesdata og instrumentelle studier.
MR har de bedste muligheder for at visualisere prostatastrukturen. Den moderne standard for undersøgelse af bækkenorganerne ved hjælp af MR-metoden er brugen af en endorektal sensor, som giver mulighed for at opnå et billede med den højest mulige rumlige opløsning på 0,5-1 mm. Ved at presse luft ind i den endorektale sensor opnås en klar visualisering af prostatakapslen, de rektoprostatiske vinkler og Denonvilliers' rektoprostatiske fascia. Brugen af en endorektal sensor i MR begrænser ikke visualiseringen af regionale lymfeknuder (op til niveauet for bifurkationen af abdominalaorta). Prostatakræft er karakteriseret ved lav signalintensitet på T-vægtede billeder mod baggrund af et højintensitetssignal fra en uændret perifer zone af kirtlen. Uregelmæssig form, diffus spredning med masseeffekt, uklare og ujævne konturer er morfologiske karakteristika for foci med lav signalintensitet i prostataens perifere zone, hvilket tyder på en neoplastisk karakter af læsionen. Ved dynamisk kontrastdannelse akkumulerer kræftfokus hurtigt kontrastmidlet i arteriefasen og fjerner det hurtigt, hvilket afspejler graden af angiogenese og dermed graden af tumormalignitet. Lav signalintensitet er også karakteristisk for fokus på postbiopsiblødninger, prostatitis, benign stromal hyperplasi i kirtelens neutrale zone, fibrøse-arforandringer, fibromuskulær hyperplasi og konsekvenser af hormon- eller strålebehandling. MR-scanning uden dynamisk kontrastdannelse tillader ikke pålidelig differentiering af de fleste af de anførte ændringer og sygdomme.
Som nævnt ovenfor er en af hovedopgaverne for enhver billeddannelsesmetode til behandling af prostatakræft at bestemme kirtellæsionens volumen og tumorens spredning ud over kapslen. Bestemmelse af tumorvolumen er vigtig for prognosen. Et tumorvolumen på mindre end 4 cm3 indikerer fjerne metastaser, og 12 cm3 indikerer en ekstremt høj sandsynlighed for metastaser. Ifølge forskning varierer nøjagtigheden af MR-scanning til at detektere foci af neoplastiske læsioner i prostata fra 50 til 90%. MR-scannings følsomhed til at bestemme lokaliseringen af prostatakræft er omkring 70-80%, mens mikroskopiske kræftfoci (foci) ikke kan detekteres ved hjælp af MR.
Den vigtigste fordel ved endorektal MR er evnen til at lokalisere neoplastiske læsioner i områder, der ikke er tilgængelige med andre diagnostiske metoder, og til at afklare tumorvækstens art og retning. For eksempel muliggør MR-scanning at detektere neoplastiske læsioner i de forreste dele af prostataens perifere zone, som ikke er tilgængelige med transrektal biopsi. Generelt supplerer MR-scanning dataene fra DRE og TRUS om tumorlokalisering betydeligt.
Endorektal MR-scanning muliggør visualisering af kirtelkapslen, vaskulære nervebundter, sædblærer, kirtelspids, periprostatisk venøs plexus og bestemmelse af lokal prævalens af kirteltumor. Det skal understreges, at kapselpenetration betragtes som et mikroskopisk tegn, og selv moderne MR-apparater (endorektal coil) er ikke i stand til at give sådanne oplysninger. Det er kun muligt at indhente data om vækst ud over kirtelkapslen.
Diagnostiske kriterier for ekstrakapsulær ekstension ved hjælp af MR:
- tilstedeværelsen af en ekstrakapsulær tumor;
- ujævn kontur af kirtlen (deformation, vinkelform);
- asymmetri af neurovaskulære bundter;
- udslettelse af de rektoprostatiske vinkler;
- bred kontakt mellem tumoren og kapslen.
Den højeste specificitet (op til 95-98%) og nøjagtighed af MR-resultater opnås ved undersøgelse af patienter med medium eller høj risiko for ekstrakapsulær invasion. Det menes, at ekstrakapsulær invasion (ifølge MR-data) indikerer uhensigtsmæssig kirurgisk behandling og en ugunstig prognose for sygdommen. Hormonal eller strålebehandling påvirker ikke nøjagtigheden af at detektere ekstrakapsulær spredning af prostatatumor. Den største vanskelighed ved at detektere kræftfokus og ekstrakapsulær spredning af tumor er den høje variation i fortolkningen af tomogrammer foretaget af forskellige specialister. Den primære opgave for en specialist i strålediagnostik er at opnå høj diagnostisk specificitet (selv på bekostning af sensitivitet) for ikke at fratage operable patienter chancen for radikal behandling.
Ligheden i tætheden af kræft-, hyperplastisk og normalt prostatavæv i CT gør denne metode ringe anvendelig til vurdering af tumorens lokale spredning. Invasion i sædblærerne er vigtigere end invasion i kapslerne, men selv i dette tilfælde giver CT kun information i fremskredne tilfælde. Denne metode bruges dog aktivt til at markere påvirkningsområdet før strålebehandling.
Den langsomme udvikling af strålediagnostik i vores land har ført til sen diagnose af prostatakræft og dermed til utilstrækkelig udbredelse af radikale metoder til behandling af prostatakræft (f.eks. prostatektomi), lav tilgængelighed af moderne tomografier og fravær af passende uddannelsesprogrammer for specialister i strålediagnostik og urologer. På trods af at CT og MR nu er udbredt, er klinikkernes udstyrsniveau og uddannelsen af specialister i strålediagnostik utilstrækkeligt til, at de indhentede oplysninger kan være afgørende for valget af en behandlingsmetode til patienter med prostatakræft.
Regionale lymfeknuder (N)
Regionale lymfeknuder bør kun vurderes, når dette direkte påvirker behandlingsstrategien (normalt ved planlægning af radikal behandling). Høje PSA-niveauer, T2c -T3a- tumorer, dårlig differentiering og perineural invasion er forbundet med en høj risiko for lymfeknudemetastase. Vurdering af lymfeknudestatus baseret på PSA-niveauer anses for utilstrækkelig.
Kun lymfadenektomi (åben eller laparoskopisk) giver den nødvendige information. Nyere undersøgelser af udvidet lymfadenektomi har vist, at prostatakræft ikke altid påvirker obturatorlymfeknuderne. Ved asymptomatiske tumorer og PSA-niveauer under 20 kg/ml bekræfter CT kun forstørrede lymfeknuder i 1% af tilfældene. Brugen af MR eller CT er berettiget i tilfælde af høj risiko for metastase, da specificiteten af disse metoder når 93-96%. Selv et positivt resultat ved brug af dem kan dog være falsk, og kun en punktering af en mistænkelig lymfeknude giver mulighed for at afvise lymfadenektomi. Ifølge retrospektiv analyse indikerer lymfeknudens størrelse ikke altid tilstedeværelsen af metastaser i den; asymmetri af de berørte lymfeknuder betragtes som et mere informativt tegn. I øjeblikket diagnosticeres kun 2-3% af patienter, der har gennemgået radikal prostatektomi for lokaliseret prostatakræft, med metastase til lymfeknuderne baseret på postoperativ histologisk undersøgelse.
Positronemissionstomografi (PET) og scintigrafi med mærkede antistoffer anbefales som metoder til at detektere metastaser til lymfeknuder, men deres anvendelse er stadig begrænset på grund af utilstrækkelig følsomhed.
Partins nomogrammer (2001) kan bruges til at vurdere risikoen for regional lymfeknudeinvolvering. Nomogrammer er matematiske algoritmer, der bruges til en specifik patient eller en gruppe af patienter. Disse tabeller gør det muligt at bestemme sandsynligheden for lokal tumorspredning (til kapsel, sædblærer) og lymfeknudeinvolvering baseret på det kliniske stadie, PSA-niveau og Gleason-indeks. De gør det især muligt at identificere en gruppe patienter med en lav (mindre end 10%) sandsynlighed for lymfeknudemetastase (med et PSA-niveau over 20 ng/md, stadie T 1-2a og Gleason-indeks 2-6); i denne gruppe er lymfeknudernes tilstand muligvis ikke specificeret før radikal behandling. Risikoen for lymfeknudemetastase kan også vurderes ved at detektere tumorområder med udtalt anaplasi (4-5 point): hvis sådanne områder findes i fire eller flere biopsier, eller de dominerer i mindst én biopsi, når risikoen 20-45%. Hos andre patienter overstiger den ikke 2,5%. Yderligere undersøgelse er ikke nødvendig i sådanne tilfælde.
Fjernmetastaser (M)
Hos 85% af patienter, der dør af prostatakræft, opdages læsioner i det aksiale skelet. Knoglemetastaser opstår på grund af kræftcellers indtrængen i knoglemarven med blodbanen, hvilket fører til tumorvækst og lysis af knoglestrukturer. Forekomsten af knoglemetastaser påvirker prognosen, og deres tidlige opdagelse advarer lægen om mulige komplikationer. I 70% af tilfældene er metastase kombineret med en stigning i aktiviteten af knogleisoenzymet alkalisk fosfatase (ALP). Bestemmelse af ALP-aktiviteten og PSA-niveauet giver os i langt de fleste tilfælde mulighed for at detektere knoglemetastaser. Ifølge multivariat analyse påvirkes disse indikatorer kun af antallet af knoglemetastaser. Det er vigtigt, at aktiviteten af knogleisoenzymet ALP afspejler graden af knogleskade mere præcist end PSA-niveauet.
Scintigrafi betragtes som den mest følsomme metode til at detektere knoglemetastaser (den er bedre end radiografi og bestemmelse af alkalisk og sur fosfataseaktivitet). Technetiumdifosfonater er bedre anvendt som radiofarmaceutisk lægemiddel, da deres akkumulering i knogler er meget mere aktiv end i blødt væv. Der er vist en korrelation mellem en semi-kvantitativ vurdering af knogleskade og overlevelse. Detektering af fjerne metastaser er mulig i ethvert organ. De forekommer oftest i ikke-regionale lymfeknuder, lunger, lever, hjerne og hud. I tilfælde af tilsvarende klager og symptomer anvendes røntgen af thorax, ultralyd, CT og MR til at detektere dem. Taktikkerne for mistanke om knoglemetastaser er præsenteret i diagrammet.
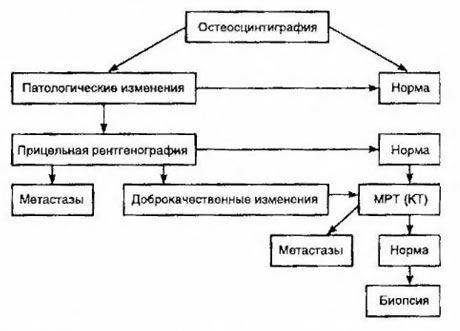
Den mest pålidelige laboratorieindikator, der hjælper med at bestemme graden af metastase, er PSA-niveauet. Det har vist sig, at en stigning over 100 ng/ml er den eneste parameter, der pålideligt indikerer fjernmetastaser. Bestemmelse af PSA-niveauet reducerer antallet af patienter, der har brug for knogleskintigrafi. Sandsynligheden for at detektere knoglemetastaser med et fald i PSA-niveauet er meget lav. I mangel af klager og med et initialt PSA-indhold på mindre end 20 ng/ml kan detektion af stærkt og moderat differentierede tumorer undgås ved scintigrafi. Samtidig er scintigrafi indiceret i tilfælde af dårligt differentierede tumorer og kapselinvasion (uanset PSA-niveauet).


 [
[