Medicinsk ekspert af artiklen
Nye publikationer
Intestinal atrofi
Sidst revideret: 07.06.2024

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
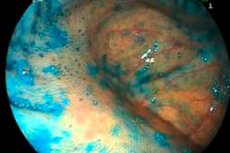
Tarmatrofi er en sekundær patologisk tilstand, der forekommer på baggrund af inflammatoriske reaktioner i tarmvæv - især med et langvarigt forløb af colitis eller enteritis. Sygdommen er kendetegnet ved periodiske akutte smerteangreb, afføringsforstyrrelser, tab af kropsvægt, generel svaghed og ubehag. I mangel af rettidig medicinsk behandling kan farlige komplikationer udvikle sig, såsom perforering, tarmobstruktion, blødning, malignisering osv. Lægerne anbefaler kraftigt, at hvis tarmatrofi er mistænkt, er det obligatorisk at kontakte den relevante specialist og gennemgå en omfattende terapi. [1]
Epidemiologi
Tarmatrofi er en temmelig almindelig patologi, der findes hos både voksne og børn. Sygdommen kombinerer elementer i den inflammatoriske proces, slimhindevævsdystrofi, hypotrofi/atrofi af glat muskel og funktionel lidelse i tarmen. Denne patologiske tilstand kan muligvis redegøre (ifølge forskellige data) for ca. 10% af alle kroniske sygdomme i fordøjelsesorganerne med en forekomst af mindst 5-12 tilfælde pr. 1 tusind befolkning.
Endoskopiske, serologiske, genetiske og morfologiske diagnostiske kapaciteter er i høj grad udvidet i løbet af de sidste par årtier. Forskere har foretaget adskillige undersøgelser, der undersøger lidelser i fordøjelseskanalen. Takket være adskillige videnskabelige værker er der ideer om denne patologi, som ikke altid er symptomatisk manifesteret og bekræftet af Laboratory, hvilket gør statistikker ekstremt vanskelige.
Tarmatrofi er aktivt undersøgt i mange år såvel som andre kroniske problemer, der påvirker den store og tyndtarm. Ikke desto mindre er der stadig ikke fuldt ud forstået. Fra perspektivet af moderne medicin betragtes tarmatrofi som et klinisk og morfologisk fænomen, der er kendetegnet ved dyspepsi og smertsyndrom med morfologisk tydelige manifestationer af vævsdystrofi/atrofi, skumning af tarmkirtler og dannelse af lymfoplasmacytisk infiltration af varierende intensitet. Der er visse vævsændringer, der er karakteristiske for tarmatrofi, men dette udtryk bruges relativt sjældent i klinisk praksis. Meget oftere kan du høre diagnosen kronisk enterocolitis, irritabelt tarmsyndrom, Crohns sygdom, ikke-specifik ulcerøs colitis.
På ICD-10-listen kan patologien kategoriseres som K52.9-ikke-infektiøse gastroenteritis og colitis uspecificeret.
Meget sjældent er medfødt atrofi af tyndtarmsmikrovilli eller mikrovillus-inklusionssyndrom en sjælden genetisk lidelse, der er arvet på en autosomal recessiv måde. Forstyrrelsen er forårsaget af medfødt atrofi af apikale mikrovilli med intracellulær ophobning af apikale enzymer i epitelstrukturer i tyndtarmen.
Hyppigheden af sygelighed kan variere meget, afhængigt af både de anvendte diagnostiske foranstaltninger og patientens vilje til at modtage medicinsk behandling. Desværre søger voksne patienter i mange tilfælde ikke lægehjælp eller søger det ikke rettidigt, men kun på scenen med komplikationer.
En speciel variant af tarmatrofi - cøliaki-sygdom - findes i en ud af hundrede mennesker i verden, selvom mange mennesker ikke søger lægehjælp, og procentdelen af mennesker med sygdommen kan være meget højere. I gennemsnit etableres en sådan diagnose ca. 5-10 år efter, at de første tegn på lidelsen vises.
Årsager Tarmatrofi
Intestinal atrofi er en multifaktoriel patologi. Der er mere end ti kendte årsager, der kan føre til atrofi af slimhindevæv og som en konsekvens af udviklingen af tarmens funktionelle svigt. Atrofiske lidelser kan være en konsekvens af patologi eller aldersinfolution. Genetisk bestemt hypotrofi eller atrofi af slimhindevævet i fordøjelsessystemet er ikke ualmindeligt.
Blandt de mest almindelige årsager til tarmatrofi anses for at være:
- Kroniske inflammatoriske processer (colitis, enteritis, enterocolitis);
- Ændringer i lokale og funktionelle forhold (dette inkluderer dårlig ernæring, stillesiddende livsstil osv.);
- Forgiftning, forgiftning;
- Hormonelle forstyrrelser i kroppen.
Derudover påvirker psyko-emotionel stress, en lang historie med rygning og alkoholmisbrug, langvarig eller hyppig brug af medicin (især antibiotika, ikke-steroide antiinflammatoriske lægemidler og kortikosteroidhormoner) tilstanden i tarmen. Sandsynlige provokerende faktorer inkluderer genetisk disponering, erhvervsmæssige farer, samtidig somatiske patologier.
Vi kan skelne de hyppigste årsager til atrofiske ændringer i vævene i forskellige dele af tarmen:
- Arvelig disponering. Hvis de nærmeste slægtninge viste sig at have tegn på tarmatrofi, øges risikoen for at få denne patologi kraftigt.
- Forkert spisevaner. Langvarig faste såvel som hyppig overspisning fører til forkert funktion af fordøjelsessystemet.
- Forbrug af lav kvalitet og usund mad. Nogle "usunde" fødevarer irriterer tarmen og bidrager til udviklingen af en kronisk inflammatorisk proces.
- Forsømmelse af kosten, der er foreskrevet af en læge som en del af behandlingen af enhver patologi i mave-tarmkanalen.
- Langvarig eller svær stress, depression, neurose.
- Langvarig antibiotikabehandling, ubalance af mikroflora i tarmen, dysbakteriose.
- Forgiftning, herunder alkoholisk forgiftning. Enhver beruselse (forgiftning) påvirker negativt vævene i fordøjelsesorganerne.
- Hypodynamia. Mangel på nødvendig fysisk aktivitet svækker muskelsystemet. Tarmens glatte muskler påvirkes også.
- Hyppig brug af afføringsmedicin.
- Uafhængig og kaotisk anvendelse af medicin, der påvirker fordøjelseskanalens arbejde og tilstand. Dette kan også omfatte forkert beregnede doser, ignorere bivirkninger.
Risikofaktorer
Når man vurderer de mulige årsager til tarmatrofi, skal det tages i betragtning, at det i de fleste tilfælde ikke handler om en, men om et helt kompleks af faktorer. I dette tilfælde kalder den førende årsag mange eksperter alimentære lidelser - det vil sige forkert ernæringsmæssig karakter og regime. Denne kendsgerning bekræftes af det faktum, at atrofiprocesserne altid er sekundære og opstår på baggrund af andre patologier. Det er ingen hemmelighed, at i henhold til de mest optimistiske beregninger i henhold til de mest optimistiske beregninger, ikke mere end 30% af mennesker, overholder en rationel diæt. Hovedparten af befolkningen overalt krænker madregimet - uordentlig spisning, spiser ofte mad "tør" og "på flugt", overspisning, samt irrationelt nærmer sig valget af diæt, spiser en masse søde, fedtholdige og krydret, misbrug af fastfood, sodavand og andre skadelige produkter. Og i de fleste tilfælde er den forkerte tilstand og arten af ernæring til stede i kombination med hinanden.
En vigtig rolle i udviklingen af tarmatrofi spiller en vigtig rolle i ormangreb og tarminfektionslæsioner - især salmonellose, desinfektion, giardiasis osv. I udviklingen af tarmatrofi. Inddragelsen af kvaliteten af mikrobiel flora fremgår af diagnosticeret dysbakteriose, som findes hos langt de fleste patienter med tarmatrofi.
Disse faktorer er de førende med hensyn til årsagerne til atrofiske processer. Oftest taler vi om disse vigtigste links for patologi:
- Alimentært forbindelse, der fører til lidelser i tarmmotilitet med yderligere udvikling af inflammatorisk reaktion;
- Infektiøs-parasitisk forbindelse, der direkte påvirker tarmvævet med den efterfølgende dannelse af dysbiose, inflammation og yderligere motoriske lidelser.
Forkert diæt, hyppighed og mængde forbruget mad, infektioner og dysbakteriose, som ofte kombineres med hinanden, abdominal traume og arvelig disponering - dette er hovedlisten for de mest sandsynlige årsager til starten af atrofiske processer.
Nogle rolle spilles også af de såkaldte psykogene faktorer, der favoriserer indtræden og yderligere forløb for den inflammatoriske reaktion. Når man indsamler anamnesis og interviewer afslører tegn på vegetovaskulær dystoni, en tendens til depression og hypokondrier. Specialister har tilstrækkelig grunde til at tro på involvering af forværret arvelighed. Hvad angår involvering af psykogene faktorer, viser det sig ofte, at patienter med tarmatrofi har øget angst og usikkerhed, følelsesmæssig labilitet og impressionsevne. På baggrund af humørsvingninger og neurose forværres intestinal motilitetsforstyrrelser og inflammatoriske reaktioner.
For gruppen af faktorer, der er gunstige for udseendet af atrofi, kan vi tilføje hypodynamia, undgå fysisk aktivitet, spise hovedsageligt raffinerede fødevarer såvel som mange dårlige vaner - primært såsom rygning og alkoholmisbrug.
Hvad angår en sådan atrofisk proces som cøliaki, er flere faktorer involveret i dens udvikling, herunder gener og kostvaner. Det er en autoimmun sygdom, hvor vævene i tyndtarmen er beskadiget på grund af forbruget af gluten. Når mennesker med visse genetiske risici spiser mad med gluten, udvikler en immunrespons i form af et respons på glutenproteiner (gliadiner og gluteniner), der angriber tyndt tarmstrukturer. Under disse angreb er de villi, der letter næringsstofabsorptionen, beskadiget. Den beskadigede villi bliver kortere og fladere og forringer signifikant absorptionen af næringsstoffer.
Mennesker med cøliaki har allelvarianter, såsom HLA-DQ2 eller HLA-DQ8. At arve disse alleler fører imidlertid ikke altid til udvikling af cøliaki og tarmatrofi. Derudover skal andre faktorer være til stede, såsom forbrug af glutenholdige fødevarer (hvede, byg, rug osv.). [2]
Patogenese
Den patogenetiske mekanisme for tarmatrofi hænger ofte sammen med lidelser i tarmbiocenose. Patologisk proinflammatorisk rolle spilles af mikrobielle aminosyrer - metaboliske produkter Scatol og Indol. På grund af øget aktivitet af opportunistisk flora øger niveauet af histamin, hvilket fører til generel sensibilisering, svækkelse af humoral og cellulær beskyttelse. Da en sådan flora perfekt tilpasser sig miljøforholdene, undertrykker den gradvist sund tarmflora. På baggrund af bifidobakteriemangel forstyrres processerne med fordøjelse, absorption og assimilering af ernæringskomponenter.
En betydelig rolle i den patogenetiske mekanisme for udvikling af tarmatrofi spilles af neuro-regulerende lidelser i organet, som er baseret på svagheden i hæmmende virkninger af cerebral cortex på de lavere sektioner med et stærkt fald i reaktiviteten af den sympatiske del af det autonome nervesystem, samt en stigning i niveauet af bioaktive stoffer - histamin og serotonin.
Et betydeligt bidrag til udvikling af atrofiske processer er en svigt i immunologisk reaktivitet. Stigning i niveauet af immunoglobuliner ledsages af udseendet af tarmens autoantistoffer i blodet, hvilket indikerer involvering af sensibilisering over for vævsantigener. Med ændringer i mikroorganismens biologiske og immunologiske egenskaber forstyrres symbiotiske forhold mellem organismen og tarmmikroflora, hvilket skaber gunstige tilstande for immunologiske lidelser. [3]
Blodcirkulationen gennemgår stærke ændringer. Vaskulære permeabilitetsændringer, manifestationer af formidlet intravaskulær koagulationssyndrom forekommer.
Tarmatrofi kan udvikle sig på grund af beruselse og giftige metaboliske processer, endokrine patologier, sygdomme i det centrale nervesystem. Problemet opstår naturligvis, når motilitetsforstyrrelser eller toksiske virkninger på tarmvæv.
Gliadin spiller en førende rolle i patogenesen af cøliaki. Dens fraktioner er giftige for mennesker med cøliaki. På samme tid spiller alfa-gliadin med 33-mer-peptid rollen som en aktivator af immunreaktion, hvilket skyldes dens modstand mod virkningerne af fordøjelsesproteinaser.
Ved cøliaki er forbruget af fødevarer, der indeholder gluten, en vigtig, men ikke den eneste faktor i udviklingen af patologien. Antigener af det vigtigste histokompatibilitetskompleks er også vigtige. Generelt har tarmatrofi ved cøliaki sygdom en multifaktoriel oprindelse. Sammen med genetisk disponering og giftig glutenindflydelse spiller interne miljøfaktorer en yderligere rolle i udviklingen af lidelsen. [4]
Symptomer Tarmatrofi
Diverse patogenetiske mekanismer til udvikling af tarmatrofi bestemmer mangfoldigheden og ikke-specificiteten af symptomatologien i patologien. Forstyrrelsen har ikke sådanne symptomer, hvorved det ville være muligt klart at bestemme tilstedeværelsen af atrofi. Desuden er det kliniske billede ofte (især i de tidlige udviklingsstadier) ekstremt sparsomt. Forløbet af sygdommen forlænges, det kan fortsætte med periodisk veksling af tilbagefald og remissioner med en gradvis forværring af problemet.
I perioder med forværring føles patienter værre, tegn på beruselse vises eller intensiveres: træthed, appetit forværres, lidt øget temperatur, generer smerter i hovedet. På samme tid forekommer mavesmerter - at ømme med en tendens til at intensivere før eller under defekationshandlingen.
Mange patienter forbinder begyndelsen eller forværringen af smertsyndrom med forbrug af mad: oftere sker det ca. 1,5 timer efter et måltid. Hvis der opstår smerter umiddelbart efter at have spist, skyldes det øget gas og abdominal oppustethed. Udledning af gas eller afføringshandlingen fører til lindring af smerter eller dens forsvinden. Generelt kan smertsyndromet beskrives som ømme, ofte forårsaget af at spise.
Ud over smertefulde fornemmelser forstyrres defekationsrytmen, ændres karakteren af fæces. Patienter rapporterer oftere forstoppelse end diarré. Afføring kan være fraværende i 1-3 dage, hvilket undertiden gør det nødvendigt at give et klyster eller tage afføringsmidler. Slim eller blod kan findes i afføringen. Arten af fæces: den såkaldte "får" eller komprimeret fecaloma. Nogle gange er der afføringsinstabilitet, ændring af forstoppelse med diarré.
Mange patienter præsenterer tegn på autonom dysfunktion og neurologiske lidelser: søvnløshed eller døsighed, irritabilitet, generel træthed, hovedpine, pulsinstabilitet.
Under ekstern undersøgelse bemærkes symptomer på kronisk beruselse. Der er plak på tungen. Abdominalområdet er oppustet, undertiden smertefuldt ved palpation. I hyperkinesi dominerer tegn på spastisk colitis og i hypokinesi - atonisk eller hypotonisk colitis.
Generelt forlænges forløbet af tarmatrofi, bølget. Andre eksisterende sygdomme i fordøjelseskanalen har en udtalt indflydelse på symptomatologien, som skal være opmærksom på under diagnosen.
Hvis atrofiske ændringer spreder sig til tarmen og maven, bemærkes sådanne symptomer som forringelse af appetit, ubehagelige bøjning og kvalme. Mange patienter rapporterer en følelse af tyngde og fylde i abdominalregionen, overdreven spyt, halsbrand og en ubehagelig eftersmag i mundhulen.
Efterhånden udvides det kliniske billede, suppleret ved at rumle i maven, intolerance over for mejeriprodukter, afføringsinstabilitet. Nogle patienter taber kropsvægt, anæmi udvikler sig, hypovitaminose, hvilket resulterer i alvorlig svaghed og træthed, åndedrætsbesvær, selv med lidt fysisk aktivitet.
Problemer med fordøjelse af mad påvirker hudens tilstand. Huden bliver tør, flager og skæl vises. På samme tid forværres immuniteten, og synet svækkes.
Første tegn
Det førende symptom på alle typer tarmatrofi er stump eller angrebslignende smerte i abdominalområdet. Den nøjagtige lokalisering af smerter afhænger af hvilket tarmsegment der påvirkes. Således kan der bemærkes smerter i navleområdet i højre iliac-region, venstre undercostal-område eller "spildt over" i hele abdominalzonen.
Der er ofte midlertidig lettelse efter gas eller en vellykket afføringshandling. Efter nogen tid vender smerten tilbage eller forværres. At tage antispasmodik eller anvende en varmekilde kan også hjælpe med at lindre smerten.
Udseendet af smerte med fysisk aktivitet eller skubbe kan indikere dybere tarmatrofi.
Andre første tegn inkluderer ofte:
- Defekationsforstyrrelser, forstoppelse skiftevis med diarré, "får" fæces;
- Lyde af "rumling" i maven, oppustethed, med en tendens til at intensivere efter måltider;
- Unormale urenheder i fæces (oftere - slim eller blod, stribet);
- En følelse af pres, tyngde i tarmområdet;
- Smertefuld tenesmus (falske trang til afføring);
- Appetit forværring og tilhørende måling;
- Subfebrile feber, hovedpine, svær træthed;
- Belching Air;
- Kvalme og opkast (sjælden).
Det kliniske billede af en sådan patologisk tilstand som cøliaki har lignende tegn:
- Gauntness;
- Skiftevis mellem forstoppelse og diarré;
- Kedelig, trækker mavesmerter;
- Ledssmerter;
- Vesikulære udslæt på huden og slimhinderne;
- Konstant og alvorlig træthed.
Symptomerne på tarmatrofi kan falde sammen med de af kronisk gastroenteritis. Forløbet af sygdommen - intermitterende, med skiftende perioder med forværringer og remissioner. Sådanne ændringer provoseres normalt af ernæringsmæssige lidelser eller eksterne stressfaktorer. Desværre, når de første tegn påvises, søger en ekstremt lille procentdel af patienter medicinsk hjælp. De fleste patienter ignorerer problemet eller selvmedicineringen, som over tid fører til forværring af patologi og udvikling af komplikationer.
Mave og tarmatrofi
Udviklingen af atrofiske processer i maven provoseres normalt af forskellige aggressive faktorer - især bakterien Helicobacter pylori, saltsyre, duodenogastrisk tilbagesvaling, pepsin, samt utilstrækkelig beskyttelse af mucosa (for eksempel med et underskud af epitelial regeneration, endnu forkert blodforsyning af organet, osv.).)
Atrofi begynder cirka 2-3 år efter starten af den inflammatoriske proces. For eksempel findes atrofiske tegn hos 43% af patienterne med kronisk gastroenterocolitis allerede 10 år efter manifestationen af patologi. Specialister taler ofte om atrofi som den sidste fase af inflammatorisk sygdom.
To hovedmekanismer er kendt for udviklingen af slimhindevævatrofi:
- Skader på grund af direkte eksponering (især bakteriel);
- En autoimmun reaktion.
Helicobacter pylori-infektion er massivt udbredt. Det forårsager skader og strukturelle ændringer i celler påvirker den beskyttende funktion af slimhinden, favoriserer og understøtter den konstante forløb af den inflammatoriske proces i vævet, hvilket indebærer atrofi. [5]
Til gengæld er den autoimmune proces forårsaget af arvelige svigt ved kroppens immunreaktivitet. Under reaktionen "antigen-antistof" er der for tidlig afgrænsning og forkert modning af nye cellulære strukturer. Dette indebærer en gradvis svækkelse af gastrinsyre, ændringer i slimhindestrukturen, et fald i produktionen af saltsyre. I fordøjelsessystemet er absorptionen af vitaminer og jern forringet, og anæmi forekommer.
Helicobacter-associeret gastritis kan provokere udviklingen af autoimmun aggression mod gastrisk epitelvæv med yderligere udvikling af atrofiske og metaplastiske processer. Patienter med detekteret Helicobacter pylori viser sig oftere at have kirtelatrofi, især udtalt ved høje titere af autoantistoffer.
I sin udvikling passerer atrofien i maven og tarmen gennem flere stadier:
- Overfladisk inflammatorisk proces udvikler sig, hydrochlorsyreproduktion lider ubetydeligt, der er ingen tegn på patologi;
- Der er fokus af atrofi;
- Diffuse ændringer med udtalt lidelser ved sekretorisk funktion forekommer (slimhindevæv er tyndere, fokus af tyndtarmsmetaplasi dannes).
Atrofi af maven og tarmene betragtes som en af de grundlæggende risikofaktorer for ondartet tumorudvikling. De vigtigste symptomer på problemet: Ændring i appetit, kvalme, ubehagelig bøjning. De fleste patienter har en følelse af tyngde og fylde i maven, spyt, halsbrand, ubehagelig smag i mundhulen bemærkes. Gradvist tilsat og andre symptomer såsom flatulens, ustabil afføring (forstoppelse erstattes af diarré). Med hyppig diarré er mulig gauntness, manifestationer af mineral- og vitaminmangel, anæmi. Som et resultat af nedsat evakuering af fødevarer kan der være generet af mavesmerter (kedelig, presse, med øget intensitet efter at have spist). Hvis ubehandlede, kan atrofiske processer forårsage udvikling af hypovitaminose og anæmi, achlorhydria, ulcerative læsioner og kræft.
Komplikationer og konsekvenser
I mangel af behandling og forsømmelse af medicinsk rådgivning øges risikoen for at udvikle de formidable komplikationer af tarmatrofi markant:
- Tyktarmskræft; [6]
- Perforering af den berørte tarmvæg;
- Komplet eller delvis tarmobstruktion;
- Cachexia;
- Massiv blødning;
- Septiske komplikationer.
Tarmatrofi kan blive så kompliceret, at patienten kræver nødsituation.
Særligt alvorlige komplikationer inkluderer:
- Giftig megacolon - overdreven udvidelse af den store tarmlumen, hvilket forårsager markant forringelse af patientens velbefindende, feberfeber, forstoppelse, flatulens, andre optrædener af beruselse.
- Massiv tarmblødning - opstår, når store kar, der leverer blod til tarmvæggen, udsættes. Mængden af blodtab kan være op til 500 ml pr. Dag.
- Perforering af den store tarmvæg - dannet på baggrund af overdreven strækning og atrofisk udtynding af væggen i det hule organ. Som et resultat udvikler det intrentestinale indhold i abdominalhulen, peritonitis.
- Kolorektal kræft - er i stand til at udvikle sig med en langvarig eksisterende atrofisk proces. Atrofi af tarmtarmen og endetarmen er især almindelig for malignisering.
Ondartet transformation diagnosticeres:
- Med et ti-årigt atrofi - i 2% af tilfældene;
- Med et 20-årigt kursus i 8% af tilfældene;
- Hvis tarmatrofi har været til stede i mere end 30 år - i 18% af tilfældene.
Diagnosticering Tarmatrofi
For at få det mest komplette billede af den eksisterende sygdom og derefter vælge den rigtige behandlingstaktik, ordinerer lægen en omfattende diagnose, herunder både laboratorie- og instrumentelle studier.
Blodprøver udføres først. Dette er nødvendigt for at identificere den inflammatoriske eller allergiske proces for at bestemme den mulige anæmi (som et resultat af blodtab), for at vurdere kvaliteten af metaboliske processer (protein, vandelektrolyt) og sandsynligheden for involvering af leveren eller andre interne organer. Også laboratoriediagnostik udføres for at vurdere effektiviteten af den foreskrevne behandling og overvåge dynamikken.
Foruden generelle og biokemiske blodprøver kan lægen ordinere en undersøgelse af indikatorerne for perinukleære cytoplasmatiske antineutrophil antistoffer (PANCA), Saccharomyces antistoffer (ASCA) og så videre.
Afføringsanalyse inkluderer coprogram, Gregersen-reaktion (bestemmer tilstedeværelsen af skjult blod). På samme tid påvises mulige urenheder i slim, pus, blod i fæces.
I nærvær af en infektiøs proces og behovet for at vælge antibakterielle lægemidler ordinerer bakteriologisk kultur og PCR.
Endoskopi er en af de vigtigste instrumentelle procedurer for tarmatrofi. Metoden kan bruges både på ambulant og ambulant basis. På den første fase af endoskopisk undersøgelse forklarer lægen til patienten, hvordan man korrekt forbereder sig til proceduren. I næsten alle tilfælde kræver forberedelse rensning af tarmhulen ved hjælp af specielle afføringsmidler, rensning af klyster eller begge dele i kombination. På dagen for den planlagte endoskopiske undersøgelse er forbudt at spise (morgenmad), er det tilladt at drikke vand. Generelt involverer teknikken introduktionen af et endoskopisk rør gennem anus, udstyret med en lysende enhed og et videokamera. Således kan specialisten visuelt undersøge tilstanden af slimhindevævet og bestemme de karakteristiske tegn på tarmatrofi. Om nødvendigt tages en biopsi - en partikel af tarmvæv - på samme tid og sendes derefter til histologisk undersøgelse.
Endoskopisk instrumental diagnose kan repræsenteres ved sådanne procedurer:
- Rektoromanoskopi ved hjælp af et stift rektoromanoskop i området med endetarmen og sigmoid kolon;
- Fibroileocolonoskopi ved anvendelse af et fleksibelt endoskop i tyktarmen og ileum;
- Fibrosigmoidoskopi ved anvendelse af et fleksibelt endoskop i endetarmen og sigmoid kolon;
- Fibrocolonoskopi ved hjælp af et fleksibelt endoskop i tyktarmen.
Varigheden af disse procedurer kan variere fra 20-30 minutter til halvanden time (f.eks. Hvis der anvendes overfladisk anæstesi).
Radiografi bestilles kun, når endoskopi ikke kan udføres af en eller anden grund.
En anden almindelig metode, irrigoskopi, involverer klysteradministration af en bariumophæng - et radiografisk kontrastmiddel - til patienten, hvorefter der tages røntgenstråler i tarmen. Efter tømning indføres luft endvidere i tarmhulen og igen tage billeder. Som et resultat får specialisten et billede af indsnævring og dilatation af tarmen, områder med betændelse eller overfladiske ændringer i slimhinden.
Gennemgå radiografi pålægges at udelukke udviklingen af komplikationer - såsom perforering eller giftig udvidelse af tarmen.
Ultralyd i tarmatrofi bruges praktisk talt ikke på grund af lav informativitet. [7]
Differential diagnose
Før lægen fortsætter til en fuldgyldig diagnose, skal lægen udelukke tilstedeværelsen i patienten med mange sygdomme, der kører med et lignende klinisk og endoskopisk billede. Blandt sådanne patologier:
- Infektiøs enterocolitis (parasitisk, bakteriel, viral etiologi);
- Crohns sygdom;
- Iskæmisk form af enterocolitis (forårsaget af en mangel på blodforsyning til tarmvæggen);
- Diverticulitis;
- Enterocolitis forårsaget af at tage visse medicin;
- Stråling Enterocolitis;
- En ondartet tumor i tyktarmen;
- Rektal ensom mavesår;
- Endometriose hos kvinder osv.
Disse sygdomme kan vise symptomatologi, der ligner den af tarmatrofi. Imidlertid er behandlingen af disse patologier grundlæggende forskellig. Derfor skal patienten ved udseendet af de første tegn på lidelsen konsultere en læge og ikke prøve at diagnosticere og behandle sygdommen på egen hånd.
Det er ofte vanskeligt at skelne mellem tarmatrofi og Crohns sygdom. Hvis der er tvivl, ordinerer lægen yderligere diagnostik:
- Immunologisk;
- Radiologisk;
- Endoskopisk.
At stille den korrekte diagnose er ekstremt vigtig, selvom mange af de præsenterede sygdomme har lignende udviklingsmekanismer. Selv i disse situationer er behandlingen altid forskellig. I sjældne tilfælde stilles en diagnose af uklassificeret (udifferentieret) enterocolitis: når der af en eller anden grund ikke er en præcis diagnose ikke kan fastlægges.
Diagnose af cøliaki er et separat problem. I modsætning til sygdomme, der er forbundet med fødevareallergi (inklusive glutenallergier), kan cøliaki ikke direkte knyttes til forbruget af glutenholdige fødevarer. Inddragelse af gluten i skaden af tarmvæv kan kun påvises i løbet af morfologisk analyse af slimhindebiopsi. Atrofi af den tyndtarme villi er karakteristisk ikke kun af cøliaki, men også af akutte tarminfektioner eller immunoglobulinmangel.
Hvad angår diverticulitis, er det en atrofi af tarmmusklerne med dens ekspansion i lavtliggende områder. Det er en kronisk patologi, hvor væggene i den store tarm danner sac-lignende buler gennem muskulaturlag. Diagnosen af diverticulitis etableres ikke, før lægen fuldstændigt udelukker tilstedeværelsen af kræft. Det er vigtigt at huske, at patienter ofte diagnosticeres med både diverticula og kolorektal kræft på samme tid. Nogle gange findes kræft og divertikulose sammen i det samme segment af tyktarmen.
Hvem skal kontakte?
Behandling Tarmatrofi
Umiddelbart efter diagnosen ordineres en patient med tarmatrofi en speciel diæt, hvilket er vigtigt at observere strengt. Specialister laver en individualiseret fødevareplan, der beskriver alle anbefalinger om sammensætningen og reglerne for madlavning, diætregime.
Medicin bruges afhængigt af indikationer og diagnostiske resultater. Hvis der påvises en smitsom proces, kan antibiotikabehandling ordineres. For at reducere smertsyndrom anvendes antispasmodik. I de fleste tilfælde er det passende at bruge lægemidler, der kan gendanne normal tarmmikroflora. Hvis angivet, kan afføringsmidler eller astringenter være påkrævet.
I perioder med inflammatorisk forværring ekskluderer krydderier, stegt og fedtholdige fødevarer, ildfaste fedtstoffer, røget kød og pølser, saucer, konserveringsmidler og marinader. Svampe og nødder, friske kager og pandekager, kaffe og kakao (inklusive chokolade), sodavand og is, fastfood og snacks, rå frugter og grøntsager, mælk og tørrede frugter er forbudt.
Anbefalede fødevarer inkluderer mejeri-fri grød baseret på ris, havregryn, boghvede, semulina. Tilladt æg, korn- og grøntsagssupper (uden passivering), hvidt magert kød og dampet havfisk, tørret lysbrød, galetter, rusks, vegetabilske kartoffelmos (inklusive kartoffel), bagt frugt uden hud (æbler eller pærer), ikke-koncentrerede komprotater og sure, ikke-akidisk naturlig gelé. Mad er dampet, kogt, pureret eller pureret, bagt, serveret varm.
I perioder med remission kan mad ikke slibes eller pureres. Introducer i diæt naturlige juice med en fortynding af vand 50/50, ikke-syrende bær, marmelade, marmelade, marshmallows, frisk agurk.
Mejeriprodukter introduceres i stabil remission. Præference gives til ikke-syrende cottage cheese af medium fedtindhold (kan være i form af gryderetter eller dampede ostekager), naturlig yoghurt og kefir. Hård ikke-skarp ost kan kun forbruges, hvis den normale funktion af defekation.
Hvis en patient diagnosticeres med cøliaki, er den vigtigste terapeutiske metode en streng livslang tilslutning til en glutenfri diæt. Diet er helt fri for hvede, rug, byg, havre i alle deres manifestationer. Så under Ban Fall-brød, pasta, havregryn, hvede eller semulje. Den positive effekt af at ændre kosten bliver mærkbar i løbet af de første par uger.
Valget af typer af konservativ og kirurgisk behandling bestemmes afhængigt af sværhedsgraden og omfanget af den atrofiske proces, effektiviteten af tidligere udført terapi, risikoen for komplikationer. [8]
Indikationer for kirurgisk intervention inkluderer:
- Fravær af den nødvendige effekt fra konservativ behandling eller umulighed af dens fortsættelse;
- Udvikling af tarmkomplikationer;
- Proces malignitet eller dens øgede risici.
Forebyggelse
Desværre tænker de fleste på deres eget helbred for sent, når sygdommen allerede udvikler sig, er der udtalt symptomer. Mange, selv at vide om tilstedeværelsen af problemet, fortsætter med at forsømme lægen fra lægen, ignorere anbefalingerne om sund kost og aktiv livsstil, i betragtning af det et spørgsmål om vanskeligheder og ineffektiv. I mellemtiden er den mest effektive forebyggelse af udviklingen af tarmatrofi bare enkel og effektiv. Det består af følgende anbefalinger:
- Spis regelmæssigt på omtrent samme tid;
- Forbruge en tilstrækkelig mængde af stuetemperaturvæske (beregning af det optimale væskemængde - fra 30 til 40 ml pr. 1 kg kropsvægt);
- Undgå slik, fødevarer med konserveringsmidler, røget kød, krydret krydderier, animalsk fedt;
- Medtag gærede mælkeprodukter, fiber, vegetabilske olier i den daglige diæt.
Det er obligatorisk at opgive velkendte dårlige vaner. Det er bevist, at alkohol og nikotin bidrager til udviklingen af inflammatoriske processer i GI-kanalen, onkologi, patologier i leveren og bugspytkirtlen, hvilket skyldes den negative indflydelse af alkoholer, toksiner, kemiske forbindelser. Vigtigt: fordøjelsesproblemer, herunder tarmatrofi, kan indirekte provokere ikke kun konventionelle cigaretter, men også hookahs, IQOS og så videre.
En anden vigtig forebyggende foranstaltning er at tage en bevidst tilgang til dit eget helbred. Selvmedicinering bør ikke praktiseres: Hvis der vises mistænkelige symptomer, er det nødvendigt at besøge din familielæge og gennemgå diagnostik. Uberettiget og forkert brug af medicin kan føre til meget uheldige konsekvenser. For eksempel kan tarmatrofi provoseres ved langvarig anvendelse af ikke-steroide antiinflammatoriske lægemidler, langvarig antibiotikabehandling, analfabet brug af kortikosteroidlægemidler. Ikke mindre farlig og alle mulige folkemusikprocedurer med uprøvet effektivitet: Denne kategori inkluderer en række såkaldte "rensning" af GI-kanalen, Tyubazhi, langvarig faste osv. Enhver af disse procedurer skal være aftalt på forhånd med en læge og udførte kun med hans tilladelse og under hans tilsyn.
For at forhindre sygdomme i maven og tarmen anbefales det at normalisere den psyko-emotionelle tilstand, undgå overarbejde, stress, overdreven reaktioner på mulige vanskelige livssituationer (afskedigelse, skilsmisse osv.). I disse situationer kan der hjælpe sessioner med meditation, rådgivningspsykolog, sportstræning, autotræning. I nogle tilfælde kan der tages særlige beroligende midler efter lægens insistering.
Forebyggelse inkluderer også kampen mod fedme: den består af ordentlig ernæring og træning. Det er kendt, at overdreven kropsvægt provokerer udseendet af problemer med bugspytkirtlen og leveren, bidrager til et fald i tarmmotilitet. For at slippe af med ekstra pund skal du omhyggeligt overveje og lave en diæt, hvis grundlag skal være grøntsager og frugter, korn, magert hvidt kød og skaldyr. En sund kost suppleres nødvendigvis med kompetent og doseret fysisk aktivitet.
Disse foranstaltninger kan gradvist stabilisere metabolismen, styrke immuniteten, mætte blodet med ilt, forbedre psyko-emotionel tilstand. Som et resultat vil en person undgå udvikling af forskellige sygdomme i fordøjelsessystemet, herunder tarmatrofi, og bevare deres eget helbred i lang tid.
Vejrudsigt
Tarmatrofi er en alvorlig patologisk ændring i tarmstrukturen. Hvis behandlingen forsømmes eller utidige terapeutiske foranstaltninger kan udvikle alvorlige komplikationer, interne blødninger, irreversible ændringer i fordøjelsessystemet.
For at forbedre prognosen for sygdommen skal du undgå yderligere morfologiske ændringer og udvikling af tyktarmskræft, anbefales det:
- Kontakt din læge mindst to gange om året;
- Udfør regelmæssigt rutinemæssig endoskopi (frekvens bestemmes af lægen afhængigt af intensiteten af morfologiske abnormiteter i tarmen);
- Tag regelmæssigt blodprøver til rettidig påvisning af anæmi og vurdering af dynamikken i behandlingen;
- Overhold den kost, der er ordineret af den deltagende læge;
- Følg alle medicin, der er foreskrevet af din læge;
- Koordiner med læger for at tage medicin, der kan påvirke tilstanden af tarmvæv.
Tarmatrofi er en sygdom, der er kendetegnet ved udtynding af tarmslimhinden, hvilket skyldes påvirkningen af negative faktorer. Oprindeligt ødelægges den inflammatoriske proces gradvist, slimhinden ødelægges ned til den ligamentøse muskulære mekanisme for den berørte del af mave-tarmkanalen. På grund af den langvarige patologiske proces, er lumen i det hule organ indsnævret, dens funktion går gradvist tabt.
Tarmatrofi ledsages af et antal ikke-specifikke symptomer, der markant forværrer patientens livskvalitet. Og nogle komplikationer kan udgøre en trussel ikke kun for helbredet, men også for patientens liv. Desværre er der ofte vanskeligheder med den rettidige etablering af den korrekte diagnose, da symptomatologien for tarmatrofi ligner andre sygdomme i dette organ. Ikke desto mindre, hvis diagnosen stilles i tide og korrekt, og den foreskrevne behandling er korrekt, kan prognosen betragtes som betinget gunstig. Det er umuligt at helbrede sygdommen fuldstændigt, men det er ofte muligt at stoppe sin videreudvikling.

