Medicinsk ekspert af artiklen
Nye publikationer
Ikke-smukkeste mykobakterier
Sidst revideret: 23.04.2024

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
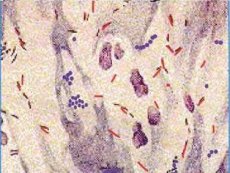
Ikke-tuberkulose mykobakterier er uafhængige arter, der er bredt fordelt i miljøet, såsom saprophytes, som i nogle tilfælde kan forårsage alvorlige sygdomme - mycobacteriosis. De kaldes også miljømæssige mykobakterier (miljømikrobakterier), mycobacteriosispatogener, opportunistiske og atypiske mykobakterier. Den væsentlige forskel mellem ikke-tuberkulose mykobakterier og mycobacterium tuberculosis kompleks er, at de praktisk talt ikke overføres fra person til person.
Ikke-tuberkulose mykobakterier er opdelt i 4 gupps ifølge et begrænset antal tegn: væksthastigheder, pigmentdannelse, koloniemorfologi og biokemiske egenskaber.
Gruppe 1 - langsomt voksende photochromogenic (M. Kansasii, etc.). Hovedmærket for repræsentanter for denne gruppe er udseendet af pigment i lyset. De danner kolonier fra S til RS-former, indeholder carotenkrystaller, som farger dem i gul. Væksthastigheden fra 7 til 20 dage ved 25, 37 og 40 ° C, katadase-positiv.
M. Kansasii - gule baciller, lever i vand, jord, påvirker oftest lungerne. Disse bakterier kan identificeres på grund af deres store størrelse og krydsformede arrangement. En vigtig manifestation af infektioner forårsaget af M. Kansasii er udviklingen af spredt sygdom. Mulige læsioner af hud og blødt væv, udvikling af tenosynovitis, osteomyelitis, lymfadenitis, perikarditis og infektioner i urogenitalt område.
2. Gruppe - langsomt voksende scotochromogen (M. Scrofulaceum, M. Matmoense, M. Gordonae, etc.). Mikroorganismer danner II mørkegult, og i lysorange eller rødlige kolonier vokser sædvanligvis S-form kolonier ved 37 ° C. Dette er den største gruppe af ikke-berusede mykobakterier. De skiller sig ud fra forurenede reservoirer og jord a og har ringe patogenicitet for mennesker og dyr.
M. Scrofulaceum (fra engelsk scrofula - scrofula) - en af hovedårsagerne til cervikal lymfadenitis hos børn under 5 år. I nærvær af alvorlige samtidige sygdomme kan de forårsage skade på lungerne, knoglerne og blødt væv. Foruden vand og jord isoleres mikrober fra rå mælk og andre mejeriprodukter.
M. Maimoense - mikroaerofiler, danner gråhvide glatte skinnende uigennemsigtige kuppelformede runde kolonier.
Primære isolater vokser meget langsomt ved 22-37 ° C. Deres udsættelse for lys forårsager ikke produktion af pigment. Om nødvendigt fortsætter eksponeringen op til 12 uger. Hos mennesker forårsager de kroniske lungesygdomme.
M. Gordonae - de mest almindelige anerkendte saprophytter, scotochromogener af vanddrivende vand, mycobacteriosis er ekstremt sjældne. Udover vand (kendt som M. Aquae) isoleres de ofte fra jord, mavesaft, bronkial sekret eller andet materiale fra patienter, men i de fleste tilfælde er de ikke-patogene for mennesker. Samtidig er der rapporter om tilfælde af meningitis, peritonitis og hudlæsioner forårsaget af denne type mykobakterier.
Den tredje gruppe er langsomt voksende nonchromogene mykobakterier (M. Avium kompleks, M. Gaslri M. Terrae kompleks, etc.). De danner farveløse S- eller SR- og R-former for kolonier, som kan have lysegul og cremefarver. De skiller sig ud fra syge dyr, fra vand og jord.
M. Avium - M. Inlracellulare kombineres i et M. Avium kompleks, fordi deres interspecifikke differentiering giver visse vanskeligheder. Mikroorganismer vokser ved 25-45 ° C, patogene for fugle, mindre patogene for kvæg, svin, får, hunde og er ikke patogene for marsvin. Oftest forårsager disse mikroorganismer en lungeskade hos en person. Huddefekter, muskelvæv og knogleskelet samt disseminerede former for sygdomme er beskrevet. De er blandt de forårsagende midler til opportunistiske infektioner, der komplicerer det erhvervede immunbristsyndrom (AIDS). M. Avium underarter af paratuberculosis er årsagsmidlet til Jones sygdom hos kvæg og muligvis Crohns sygdom (kronisk inflammatorisk sygdom i mave-tarmkanalen) hos mennesker. Mikroben er til stede i kød, mælk og afføring af inficerede køer, og findes også i vand og jord. Standard vandrensningsmetoder inaktiverer ikke denne mikrobe.
M. Xenopi forårsager lungeskader hos mennesker og formidlede former for AIDS-relaterede sygdomme. De er adskilt fra frøer af slægten Xenopus. Bakterier danner små, glatte og skinnende overflader, som ikke er pigmenterede kolonier, der efterfølgende farves i en lysegul farve. Termofiler vokser ikke ved 22 ° C og giver god vækst ved 37 og 45 ° C. På en bakterioskopi ligner meget tynde sticks, aftagende fra den ene ende og placeret parallelt med hinanden (og en slags palisade). De isoleres ofte fra koldt og varmt vand fra vandet, herunder drikkevand, der opbevares i hospitalsbeholdere (nosokomielle udbrud). I modsætning til andre betinget patogene mykobakterier er de følsomme for virkningen af de fleste anti-tuberkulosemediciner.
M. Ukerans - etiologisk middel af mycobakteriel kutan N (Buruli ulcer), vokser kun ved 30-33 ° C, kolonitilvækst forekommer først efter 7 uger. Udskillelsen af patogenet forekommer også, når musene er inficeret i kødet af fodsålen. Denne sygdom er almindelig i Australien og Afrika. Kilden til infektion er det tropiske miljø og vaccination med BCG vaccine fra denne mycobacteriosis.
Den fjerde gruppe er hurtigt voksende mykobakterier (M. Fortuitum-kompleks, M. Phlei, M. Xmegmatis, etc.). Deres vækst er noteret i form af R- eller S-former for kolonier i 1-2 til 7 dage. De findes i vand, jord, spildevand og er repræsentative for den normale mikroflora af menneskekroppen. Bakterier fra denne gruppe er sjældent isoleret fra patologisk materiale fra patienter, men nogle af dem er af klinisk betydning.
M. Fortuitum-komplekset omfatter M. Fortuitum og M. Chcionae, som består af underarter. De forårsager disseminerede processer, hud- og postoperative infektioner, lungesygdomme. Mikroberne i dette kompleks er stærkt resistente over for anti-tuberkulosemediciner.
M smegmatis - en repræsentant for normal mikroflora, skiller sig ud fra smæma hos mænd. Det vokser godt ved 45 ° C. Som et årsagsagent for menneskelige sygdomme er det andet blandt hurtigt voksende mykobakterier efter M. Fortuitum-komplekset. Det påvirker huden og blødt væv. Kræftfremkaldende midler af tuberkulose skal differentieres fra M. Smegmatis i undersøgelsen af urin.
De mest almindelige mykobakterier er forårsaget af repræsentanter for 3. Og 1. Gruppe.
Epidemiologi af mykobakterier
Mycobacteriosis patogener er udbredt i naturen. De kan findes i jord, støv, tørv, mudder, vand i floder, reservoirer og svømmebassiner. De findes i mider og fisk, fordi sygdomme hos fugle, vildt og husdyr er repræsentanter for den normale mikroflora af slimhinderne i det øvre luftveje og urinvejen hos mennesker. Infektion med ikke-tuberkulose mykobakterier opstår fra miljøet aerogent ved kontakt med skader på huden samt mad og vandveje. Overførslen af mikroorganismer fra person til person er ukarakteristisk. Disse betingelsesmæssige patogene bakterier, så den store betydning i sygdommens fremkomst har et fald i makroorganismens modstand, dens genetiske prædisponering. I de berørte områder dannes granulomer. I alvorlige tilfælde er phagocytose ufuldstændig, bakteriemæmi udtrykkes, og makrofager fyldt med ikke-tuberkuløse mykobakterier og ligner spedalceller identificeres i organerne.
Symptomer på Mycobacterioses
Symptomer på mykobakterier er forskellige. Ofte påvirkes luftvejene. Symptomatologien i lungepatologien ligner den af tuberkulose. Der er imidlertid tilfælde ekstrapulmonal proces, der involverer hud og subkutane væv, sår overflader, lymfeknuder og de urogenitale organer, knogler og led og meninges. Organ skade kan begynde både akut og i hemmelighed, men næsten altid fortsætte hårdt,
Det er også muligt at udvikle en blandet infektion (blandingsinfektion), i en række tilfælde kan de forårsage udviklingen af en sekundær endogen infektion.
Mikrobiologisk diagnose af mykobakterier
Den vigtigste metode til diagnosticering af mycobacteriosis bakteriologisk. Materialet til undersøgelsen er taget, baseret på patogenesen og kliniske manifestationer af sygdommen. Indledningsvis afgøres spørgsmålet om tilhørsforholdet til den isolerede rene kultur til patogenerne af tuberkulose eller ikke-tuberkuløse mykobakterier. Derefter anvendes et sæt undersøgelser til bestemmelse af typen af mykobakterier, graden af virulens og Runyon-gruppen. Primæridentifikation er baseret på sådanne egenskaber som væksthastighed, evne til at danne pigment, koloniernes morfologi og evnen til at vokse ved forskellige temperaturer. For at identificere disse tegn er der ikke behov for yderligere udstyr og reagenser, så de kan bruges i de grundlæggende laboratorier af TB dispensarer. Endelig identifikation (referenceidentifikation) ved brug af komplekse biokemiske undersøgelser udføres i specialiserede moratorier af videnskabelige institutioner. I de fleste tilfælde foretrækkes deres identifikation ved biokemiske fakta, som moderne molekylære genetiske metoder er arbejdskrævende, har mange forberedende faser, kræver særligt udstyr, dyrt. Af stor betydning for bagning er definitionen af følsomhed overfor antibiotika. Kritisk til diagnosen mycobacteriosis er kriteriet for samtidig udseende af kliniske, radiologiske, laboratoriedata og isoleringen af en ren kultur af ikke-tuberkulose mykobakterier, der gennemfører flere studier i dynamik.
En hjælpeværdi ved diagnosen er definitionen af antitese ved hjælp af RNGA, RP, immunoelektroforese, RNIF og ELISA, samt indstilling af hudallergiske test med sensiner.
Behandling og specifik forebyggelse af mykobakterier
Alle typer af ikke-berusede mykobakterier, undtagen M. Xenopi, er resistente over for isoniazil, streptomycin og thiosemicarbazon. Behandling af mykobakterier med anti-tuberkulose og antibakterielle lægemidler bør være lang (12-13 måneder) og kombineret. Normalt er det ineffektivt med MAC-smitsomme sygdomme og sygdomme forårsaget af hurtigt voksende mykobakterier. I nogle tilfælde anvendes kirurgisk behandling. Forberedelser til specifik forebyggelse af mycobakterier er ikke blevet udviklet.


 [
[