Medicinsk ekspert af artiklen
Nye publikationer
Hjerteklapper
Sidst revideret: 04.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Man troede tidligere, at alle hjerteklapper var simple strukturer, hvis bidrag til ensrettet blodgennemstrømning blot var passiv bevægelse som reaktion på en påført trykgradient. Denne forståelse af "passive strukturer" førte til udviklingen af "passive" mekaniske og biologiske klapperstatninger.
Det bliver nu tydeligt, at hjerteklapper har en mere kompleks struktur og funktion. Derfor forudsætter skabelsen af en "aktiv" hjerteklap-erstatning en betydelig lighed i struktur og funktion med den naturlige hjerteklap, hvilket i fremtiden er ret realistisk takket være udviklingen af vævsteknologi.
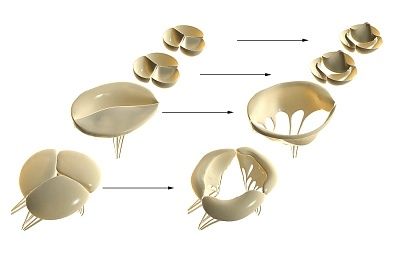
Hjerteklapper udvikles fra embryonale rudimenter af mesenkymalt væv under dannelsen af endokardiet. Under morfogenesen dannes den atrioventrikulære kanal (trikuspidal- og mitralklapper) og den ventrikulære udstrømningskanal (aorta- og pulmonalklapper).
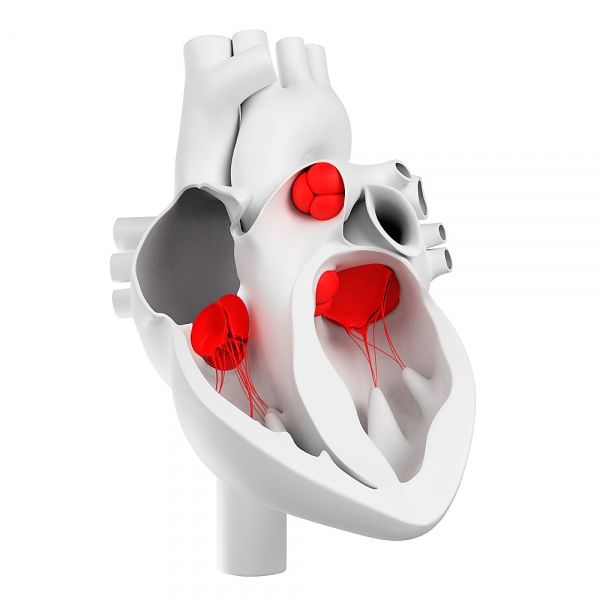
Hvordan er hjerteklapper arrangeret?
Undersøgelsen af blodforsyningen til klapperne blev initieret af N. Luschka (1852), som injicerede hjertekarrene med en kontrastmasse. Han opdagede adskillige blodkar i klappernes og de halvlunære klapper i aorta og lungearterien. Samtidig indeholdt en række manualer om patologisk anatomi og histologi indikationer på, at uændrede menneskelige hjerteklapper ikke indeholder blodkar, og sidstnævnte optræder kun i klapperne i forskellige patologiske processer - åreforkalkning og endokarditis af forskellige ætiologier. Oplysninger om fraværet af blodkar var hovedsageligt baseret på histologiske undersøgelser. Det blev antaget, at i fraværet af blodkar i den frie del af klapperne sker deres ernæring ved at filtrere væske fra blodplasmaet, der vasker klapperne. Penetration af et par kar sammen med fibre af tværstribet muskelvæv ind i klappernes og senebåndenes baser blev bemærket.
Når man imidlertid injicerede hjertekar med forskellige farvestoffer (indisk blæk i gelatine, vismut i gelatine, vandig suspension af sort indisk blæk, opløsninger af karmin eller trypanblåt), viste det sig, at karrene trænger ind i de atrioventrikulære hjerteklapper, aortaklapperne og lungearterien sammen med hjertemuskelvævet, lidt før de når klappens frie kant.
I det løse fibrøse bindevæv i atrioventrikulære klapcusper fandtes individuelle hovedkar, der anastomoserede med kar i tilstødende områder af hjertets tværstribede muskelvæv.
Det største antal blodkar var placeret ved basen og et forholdsvis mindre antal i den frie del af disse klapper.
Ifølge KI Kulchitsky et al. (1990) findes der en større diameter af arterielle og venøse kar i mitralklappen. Ved bunden af denne klap's kupler er hovedsageligt hovedkarrene placeret med et smalt sløjfe-netværk af kapillærer, der trænger ind i den basale del af kuplen og optager 10% af dens areal. I trikuspidalklappen har arteriekarrene en mindre diameter end i mitralklappen. I denne klap's kupler er der hovedsageligt spredte kar og forholdsvis brede sløjfer af blodkapillærer. I mitralklappen forsynes den forreste kup mere intensivt med blod, i trikuspidalklappen - de forreste og bagerste kupler, som udfører den primære lukkefunktion. Forholdet mellem diametrene af de arterielle og venøse kar i de atrioventrikulære klapper i hjertet hos voksne mennesker er 1:1,5. Kapillærsløjferne er polygonale og er placeret vinkelret på bunden af klappernes kupler. Karrene danner et plant netværk placeret under endotelet på atriesiden. Blodkar findes også i senebåndene, hvor de trænger ud fra papillarmusklerne i højre og venstre ventrikel i en afstand på op til 30% af senebåndenes længde. Talrige blodkar danner bueformede løkker ved bunden af senebåndene. Hjerteklapperne i aorta og pulmonalstammen adskiller sig betydeligt fra atrioventrikulærklapperne med hensyn til blodforsyning. Hovedkarrene med en relativt mindre diameter nærmer sig bunden af aortaklappernes halvmåneformede cusper og pulmonalstammeklapperne. De korte grene af disse kar ender i kapillærløkker med uregelmæssig oval og polygonal form. De er hovedsageligt placeret nær bunden af halvmåneformede cusper. De venøse kar ved bunden af aorta- og pulmonalklapperne har også en mindre diameter end dem ved bunden af atrioventrikulærklapperne. Forholdet mellem diametrene af de arterielle og venøse kar i aorta- og pulmonalklapperne i hjertet hos voksne mennesker er 1:1,4. Korte laterale grene strækker sig fra de større kar og ender i kapillærløkker med uregelmæssig oval og polygonal form.

Med alderen sker der en forgrovning af bindevævsfibre, både kollagen og elastisk, samt et fald i mængden af løst fibrøst uformet bindevæv, og der udvikles sklerose af vævet i atrioventrikulærklapperne og halvmåneklapperne i aorta- og pulmonalarterieklapperne. Længden af de tværstribede hjertemuskelfibre i klapperne falder, og følgelig mindskes deres mængde og antallet af blodkar, der trænger ind i hjerteklapperne. På grund af disse ændringer mister hjerteklapperne deres elastiske og modstandsdygtige egenskaber, hvilket påvirker mekanismen for klapplukning og hæmodynamikken.
Hjerteklapperne har netværk af lymfekapillærer og et lille antal lymfekar udstyret med klapper. De lymfekapillærer i klapperne har et karakteristisk udseende: deres lumen er meget ujævn, den samme kapillær har forskellig diameter på forskellige steder. På steder, hvor flere kapillærer smelter sammen, dannes der udvidelser - lakuner af forskellig form. Netværkenes løkker er ofte uregelmæssige polygonale, sjældnere ovale eller runde. Ofte er lymfenetværkenes løkker ikke lukkede, og lymfekapillærerne ender blindt. Lymfekapillærernes løkker er oftest orienteret i retning fra klappens frie kant til dens base. I nogle tilfælde blev der fundet et tolags netværk af lymfekapillærer i klappernes løkker.
De endokardielle nerveplexuser er placeret i deres forskellige lag, hovedsageligt under endotelet. Ved den frie kant af klappernes spidser er nervefibrene hovedsageligt placeret radialt og forbundet med senefibrene i de senekorder. Tættere på spidsernes base dannes en stormasket nerveplexus, som er forbundet med plexusen omkring de fibrøse ringe. På de halvmåneformede spidser er det endokardielle nervenetværk mere sparsomt. På klappernes fæstested bliver det tæt og flerlagsagtigt.
Cellulær struktur af hjerteklapper
Klapinterstitielle celler, der er ansvarlige for at opretholde klappens struktur, er aflange i form med adskillige fine udløbere, der strækker sig gennem hele klapmatrixen. Der er to populationer af klapinterstitielle celler, der adskiller sig i morfologi og struktur; den ene har kontraktile egenskaber og er karakteriseret ved tilstedeværelsen af kontraktile fibriller, den anden har sekretoriske egenskaber og har et veludviklet endoplasmatisk reticulum og Golgi-apparat. Den kontraktile funktion modstår hæmodynamisk tryk og understøttes yderligere af produktionen af både hjerte- og skeletkontraktile proteiner, som inkluderer de tunge kæder af alfa- og beta-myosin og forskellige isoformer af troponin. Kontraktion af hjerteklappens blad er blevet påvist som reaktion på en række vasoaktive stoffer, hvilket tyder på en koordineret biologisk stimulus for vellykket klapfunktion.
Interstitielle celler er også essentielle komponenter i reparationssystemet i strukturer som hjerteklapper. Den konstante bevægelse af klapfligene og den tilhørende bindevævsdeformation producerer skader, som de klapinterstitielle celler reagerer på for at opretholde klappens integritet. Reparationsprocessen synes at være afgørende for normal klapfunktion, og fraværet af disse celler i nuværende kunstige klapmodeller er sandsynligvis en medvirkende faktor til den strukturelle skade på bioproteser.
Et vigtigt forskningsområde inden for interstitielle celler er studiet af interaktioner mellem dem og den omgivende matrix medieret af fokale adhæsionsmolekyler. Fokale adhæsioner er specialiserede celle-matrix-interaktionssteder, der forbinder cellecytoskelettet med matrixproteiner via integriner. De fungerer også som signaltransduktionssteder, der videresender mekanisk information fra den ekstracellulære matrix, som kan fremkalde reaktioner, herunder, men ikke begrænset til, celleadhæsion, migration, vækst og differentiering. Forståelse af cellebiologien i klapinterstitielle celler er afgørende for at belyse de mekanismer, hvorved disse celler interagerer med hinanden og deres omgivelser, så denne funktion kan genskabes i kunstige klapper.
I forbindelse med udviklingen af en lovende retning inden for vævsteknologi af hjerteklapper udføres undersøgelser af interstitielle celler ved hjælp af en bred vifte af teknikker. Tilstedeværelsen af cellecytoskelettet bekræftes ved farvning for vimentin, desmin, troponin, alfa-actin og glatmuskelmyosin, tunge kæder af alfa- og beta-myosin, lette kæder-2 af hjertemyosin, alfa- og beta-tubulin. Cellekontraktilitet bekræftes ved et positivt respons på adrenalin, angiotensin II, bradykinin, carbachol, kaliumchlorid, endotel I. Cellulære indbyrdes relationer bestemmes ved funktionelle gap-interaktioner og verificeres ved mikroinjektioner af carboxyfluorescein. Matrixsekretion etableres ved farvning for prolyl-4-hydroxylase/kollagen type II, fibronektin, chondroitinsulfat, laminin. Innervation etableres ved den tætte placering af motoriske nerveender, hvilket afspejles i aktiviteten af neuropeptid Y tyrosinhydroxylase, acetylcholinesterase, vasoaktivt intestinalt polypeptid, substans-P, capsicum-genrelateret peptid. Mitogene faktorer estimeres ved hjælp af blodpladeafledt vækstfaktor, basisk fibroblastvækstfaktor, serotonin (5-HT). De undersøgte interstitielle cellefibroblaster er karakteriseret ved en ufuldstændig basalmembran, lange, tynde cytoplasmatiske processer, tæt forbindelse med matrixen, et veludviklet ujævnt endoplasmatisk reticulum og Golgi-apparat, et rigt antal mikrofilamenter og dannelse af adhæsive bindinger.
Klapceller i endokardiet danner en funktionel, atrombogen kappe omkring hver hjerteklap, svarende til det vaskulære endotel. Den udbredte metode til klapudskiftning eliminerer endokardiets beskyttende funktion, hvilket kan føre til aflejring af blodplader og fibrin på kunstige klapper, udvikling af bakteriel infektion og vævsforkalkning. En anden sandsynlig funktion af disse celler er reguleringen af de underliggende klapinterstitielle celler, svarende til reguleringen af glatte muskelceller af endotelet. Der eksisterer komplekse interaktioner mellem endotelet og tilstødende celler, delvist medieret af opløselige faktorer, der udskilles af endotelcellerne. Disse celler danner en enorm overflade dækket af mikrofremspring på den luminale side, hvilket øger eksponeringen og den mulige interaktion med metaboliske stoffer i det cirkulerende blod.
Endotelet udviser ofte morfologiske og funktionelle forskelle forårsaget af forskydningsspændinger på karvæggen på grund af blodgennemstrømning, og dette gælder også for de klapformede endokardiale celler, som enten antager en aflang eller polygonal form. Ændringer i cellestrukturen kan forekomme på grund af virkningen af lokal hæmodynamik på komponenter i cellecytoskelettet eller sekundære effekter forårsaget af ændringer i den underliggende ekstracellulære matrix. På det ultrastrukturelle niveau har klapformede endokardiale celler intercellulære forbindelser, plasmavesikler, et groft endoplasmatisk reticulum og et Golgi-apparat. Selvom de producerer von Willebrand-faktor både in vivo og in vitro, mangler de Weibel-Palade-legemer (specifikke granuler indeholdende von Willebrand-faktor), som er organeller, der er karakteristiske for det vaskulære endotel. Klapformede endokardiale celler er karakteriseret ved stærke forbindelser, funktionelle gap-interaktioner og overlappende marginale folder.
Endokardiale celler bevarer deres metaboliske aktivitet selv in vitro: de producerer von Willebrand-faktor, prostacyclin, nitrogenoxidsyntase, udviser angiotensin-konverterende enzymaktivitet og udskiller intensivt adhæsionsmolekylerne ICAM-1 og ELAM-1, som er vigtige for binding til mononukleære celler under udviklingen af et immunrespons. Alle disse markører bør tages i betragtning, når man dyrker en ideel cellekultur til at skabe en kunstig hjerteklap ved hjælp af vævsteknologi, men det immunstimulerende potentiale af selve hjerteklap-endokardiale celler kan begrænse deres anvendelse.
Hjerteklappernes ekstracellulære matrix består af fibrøst kollagen og elastin-makromolekyler, proteoglykaner og glykoproteiner. Kollagen tegner sig for 60 % af klappens tørvægt, elastin for 10 % og proteoglykaner for 20 %. Kollagenkomponenten giver klappens primære mekaniske stabilitet og er repræsenteret af kollagener af type I (74 %), II (24 %) og V (2 %). Bundter af kollagentråde er omgivet af en elastinskede, som medierer interaktioner mellem dem. Glykosaminoglykan-sidekæderne i proteoglykanmolekyler har en tendens til at danne et gellignende stof, hvor andre matrixmolekyler interagerer for at danne permanente bindinger, og andre komponenter aflejres. Glykosaminoglykaner i menneskelige hjerteklapper består hovedsageligt af hyaluronsyre, i mindre grad af dermatansulfat, chondroitin-4-sulfat og chondroitin-6-sulfat, med en minimal mængde heparansulfat. Ombygning og fornyelse af matrixvæv reguleres af matrixmetalloproteinaser (MMP'er) og deres vævshæmmere (TI'er). Disse molekyler er også involveret i en bredere vifte af fysiologiske og patologiske processer. Nogle metalloproteinaser, herunder interstitielle kollagenaser (MMP-1, MMP-13) og gelatinaser (MMP-2, MMP-9) og deres vævshæmmere (TI-1, TI-2, TI-3), findes i alle hjerteklapper. Overdreven produktion af metalloproteinaser er karakteristisk for patologiske tilstande i hjerteklappen.
 [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Hjerteklapper og deres morfologiske struktur
Hjerteklapper består af tre morfologisk forskellige og funktionelt signifikante lag af bladmatrixen: fibrøse, svampede og ventrikulære.
Det fibrøse lag danner en belastningsbestandig ramme for klappens blad, bestående af lag af kollagenfibre. Disse fibre er arrangeret radialt i folder for at tillade arterieklapperne at strække sig, når de lukker. Det fibrøse lag ligger nær den ydre udløbsflade af disse klapper. Det fibrøse lag i de atrioventrikulære klapper fungerer som en fortsættelse af kollagenbundterne i chordae tendineae. Det er placeret mellem det svampede (indløbs-) og ventrikulære (udløbs-) lag.
Mellem det fibrøse og ventrikulære lag ligger det svampede lag (spongiosa). Det svampede lag består af dårligt organiseret bindevæv i et viskøst medium. De dominerende matrixkomponenter i dette lag er proteoglykaner med tilfældigt orienteret kollagen og tynde lag af elastin. Sidekæderne i proteoglykanmolekylerne bærer en stærk negativ ladning, hvilket påvirker deres høje evne til at binde vand og danne en porøs matrixgel. Matrixens svampede lag reducerer mekanisk stress i hjerteklappernes blade og bevarer deres fleksibilitet.
Ventrikulærlaget er meget tyndere end de andre og er rigt på elastiske fibre, der gør det muligt for vævet at modstå konstant deformation. Elastin har en svampet struktur, der omgiver og forbinder kollagenfibre og holder dem i en neutral foldet tilstand. Ventrikulært indløbslag (ventrikulært - for arterielle klapper og svampet - for atrioventrikulært) indeholder mere elastin end udløbslaget, hvilket sørger for blødgøring af det hydrauliske stød, når klapperne lukker sig. Dette forhold mellem kollagen og elastin gør det muligt for klapperne at strække sig op til 40% uden stabil deformation. Når de udsættes for en lille belastning, er kollagenstrukturerne i dette lag orienteret i belastningens retning, og dets modstandsdygtighed over for yderligere belastningsvækst øges.
Ideen om hjerteklapper som simple endokardielle duplikationer er således ikke blot forenklet, men også i bund og grund forkert. Hjerteklapper er komplekse organer, der omfatter tværstribede muskelfibre, blod- og lymfekar samt nerveelementer. Både i deres struktur og i deres funktion er klapperne en integreret del af alle hjertestrukturer. Analyse af normal klapfunktion skal tage hensyn til dens cellulære organisation samt cellernes interaktion med hinanden og matrixen. Den viden, der opnås fra sådanne studier, er førende inden for design og udvikling af klapproteser ved hjælp af vævsteknologi.

