Medicinsk ekspert af artiklen
Nye publikationer
Gliom i hjernen
Sidst revideret: 07.06.2024

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
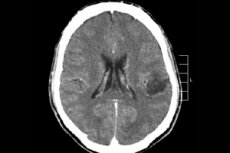
Blandt de mange tumorprocesser i centralnervesystemet diagnosticeres hjerne glioma oftest - dette udtryk er kollektiv, neoplasmaet kombinerer al diffus oligodendroglial og astrocytisk foci, astrocytom, astroblastoma og så videre. En sådan tumor kan have en anden grad af malignitet, dannes fra glialstrukturer - celler lokaliseret omkring neuroner. Hovedområdet med placering af gliomas er cerebrale halvkugler, vægge i hjerneventriklerne og chiasma - området med delvis skæringspunkt mellem optiske nervefibre. Eksternt er tumoren et nodulært element af lyserød eller rødlig farvetone, rund eller spindelformet konfiguration med utydelige grænser. [1]
Epidemiologi
I ca. 5% af tilfældene er gliomas forbundet med arvelige patologier - især neurofibromatose og andre syndromer med dominerende arv. Eksperter påpeger, at det absolutte flertal af hjerne gliomas udvikler sporadisk - det vil sige uden en klar årsag.
Generelt tegner de primære neoplasmer i det centrale nervesystem ca. 2% af alle tumorer eller lidt over 21 tilfælde pr. Hundrede tusind befolkning. Blandt dem forekommer gliomas i 35-36% af tilfældene, og mere end 15% af dem er glioblastomas.
Ifølge nogle data påvirker glioma mænd oftere end kvinder - tumoren er især almindelig blandt mennesker over 50 år gamle.
Den globale forekomst af gliomer blandt ældre er steget markant i de seneste årtier. Årsagerne til dette fænomen er endnu ikke etableret.
I henhold til definitionen af Verdenssundhedsorganisationen er tre hovedvarianter af glialtumorer, der adskiller sig i deres histologiske egenskaber, blevet identificeret. Dette er oligodendrogliomas, astrocytomer og kombinerede oligoastrocytomer. Forekomsten af hver undertype af lav malign patologi er ikke blevet pålideligt bestemt. Nogle undersøgelser indikerer en stigning i forekomsten af oligodendrogliomas fra 5% til 30% og et fald i forekomsten af astrocytomer.
Glial tumorer er i stand til at infiltrere hjernevæv, og langt de fleste af lav kvalitet bliver maligne inden for få år. [2]
Årsager Hjernegliomer
Brain Glioma er en hel gruppe tumorprocesser, hvis fælles træk er deres dannelse fra glialstrukturer af CNS, der er placeret i hjernevævet. Sådanne tumorer er opdelt i to histopatologiske varianter: høje ondartede og lave maligne gliomas.
Kilden til vækstdannelse er neuroglia-celler (astrocytter, oligodendrocytter), der giver det strukturelle grundlag og levedygtighed af hjernens neuroner.
Glial tumorprocesser adskiller sig meget i struktur, mutationsændringer i gener, aggressivitet, kliniske træk, diagnostiske egenskaber, respons på behandling og prognose for patienter. Embryonale og ependymale neoplasmer i det centrale nervesystem - især medulloblastomer og ependymomer - adskiller sig i deres histologiske struktur, men er ens med hensyn til behandling.
Glialelementer blev først klassificeret som en separat strukturel kategori af nervesystemet i slutningen af det 19. århundrede.
Neuroglia-væv består af celler, der har hjælpefunktioner: trofisk, støtte, beskyttende, sekretorisk. Neuroner og gliocytter findes sammen med hinanden, de danner sammen nervesystemet og er af stor betydning i de generelle processer i organismenes vigtige aktivitet.
Gliocytter er omtrent kategoriseret i flere større former: astrocytter, oligodendrocytter, ependymale celler og mikroglia.
Indtil videre kan forskere ikke besvare spørgsmålet om de pålidelige årsager til dannelse af neuroglial tumor. Formodentlig ydes et bestemt negativt bidrag af radioaktive effekter, infektionssygdomme, beruselse (især kemisk, erhvervsmæssig). Den arvelige faktor er også vigtig.
Hjerne gliomas opstår fra unormale neurogliocytter, der har en genetisk defekt, der fører til unormal vækst og funktionalitet - sådanne strukturer kaldes "umodne". Ufuldstændige celler er oftere placeret i et område, hvor tumoren dannes.
Kort sagt er glialdannelse resultatet af kaotisk og sporadisk vækst af modificerede neuroglia-celler. Processen kan udvikle sig fra ependymocytter, oligodendrocytter, astrocytter (astrocytom, inklusive gigantcelle og anaplastisk). [3]
Risikofaktorer
På trods af det faktum, at eksperter ikke nøjagtigt kan karakterisere årsagerne til dannelsen af glial onkopatologier, kan deres udseende i nogle tilfælde forhindres ved at eliminere de vigtigste risikofaktorer:
- Ioniserende eksponering for stråling har kræftfremkaldende aktivitet, kan forårsage udvikling af leukæmi og dannelsen af kræftprocesser med en tæt struktur, herunder hos personer i ung alder. Hyppige og urimelige radiologiske medicinske procedurer hører ultraviolet stråling (inklusive solarium) også til potentielle kræftfremkaldende virkninger og kan forårsage udseendet af tumorer i forskellige organer, herunder hjernen.
- Erhvervsmæssige bivirkninger, beruselser har ofte en årsagssammenhæng med udviklingen af kræftvulster. Produktionen af gummi og glas, pesticider og brændstoffer, metaller og tekstiler, maling og laboratorieaktenter betragtes som særlig farlige. I fare er arbejdstagere inden for aerospace-, kul- og metalindustrien, kemiske og biproduktfremstillingsanlæg, byggematerialer og elektroder, brændstoffer og smøremidler, plast og monomerer.
- Luft, vand og jordforurening er ansvarlige for op til 4% af alle kræftpatologier i verden. Karcinogener, der er til stede i store mængder i miljøet, går ind i kroppen med inhaleret luft, drikkevand og mad. At bo i økologisk usikre områder - nær store industrielle faciliteter, travle transportudvekslinger - betragtes som især farlige.
- Infektiøse patologier - især virusinfektioner - kan også skabe betingelser, der er gunstige for udviklingen af tumorer. Det er vigtigt at huske dette og at blive vaccineret på forhånd såvel som at forhindre infektions- og parasitiske sygdomme.
- Tobaks- og alkoholforgiftning betragtes som risikofaktorer for mange kræftvarianter, ikke kun hjerne gliomas.
- Utilstrækkelig fysisk aktivitet, overvægt, forkert ernæring, metaboliske lidelser, hovedskader, vaskulære patologier - yderligere stressfaktorer, der kan provokere starten på intracellulære lidelser.
- Ældre alder er den mest almindelige periode for udviklingen af neoplasmer i kroppen, så de over 55 år bør tage særlig pleje af deres eget helbred.
Imidlertid forbliver den vigtigste og mest markante risikofaktor for gliomaudvikling arvelig disponering.
Patogenese
Til dato har eksperter en række antagelser om udviklingen af hjerne gliomas. Hver teori har sine egne grunde, men den eneste korrekte og pålidelige patogenetiske mekanisme har forskere endnu ikke identificeret. I de fleste tilfælde taler vi om følgende faktorer i udviklingen af neoplasmer:
Embryogenese-fiasko, der består i forstyrrelse af organindlægning og dannelsen af "forkerte" cellestrukturer;
- Eksponering for ioniserende stråler, potentielle kræftfremkaldende stoffer i form af kemiske midler, fødevaretilsætningsstoffer osv.;
- Hovedtraume;
- Genforstyrrelser overført fra generation til generation ("familiær" glioma);
- Immundysfunktion, neuroinfektioner.
De fleste gliomer har diffus vækst med penetration i det omgivende normale hjernevæv. Afhængig af graden af malignitet kan tumoren udvikle sig i flere år uden nogen manifestation. I tilfælde af aggressivt kursus stiger symptomatologien hurtigt over flere måneder.
En del af tumorigenese skyldes dysembryogenetiske ændringer.
Hjernestammen kan påvirkes på forskellige niveauer: diffus hjernestamme glioma vil på sin side afvige både anatomo-morfologisk og klinisk. Nogle sådanne neoplasmer - især glioma af quadriplegia-pladen - kan være relativt godartet uden tegn på progression. En pontin glioma er på den anden side kendetegnet ved dens særlige malignitet, aggressivitet og dårlig prognose.
Diffuse læsioner af hjernestrukturer, hvor mere end tre anatomiske zoner i de store halvkugler er involveret i den patologiske proces, med mulig periventrikulær divergens og passage gennem corpus call gliomatosis. [4]
Er hjernes glioma arvelig?
En velprøvet risiko for dannelse af hjerne gliom er arvelig - det vil sige tilstedeværelsen af lignende eller andre intracerebrale tumorer i direkte forfædre eller i samme generation. Radioaktive eksponeringer og regelmæssig eller langvarig kontakt med potentielle kræftfremkaldende stoffer forværrer situationen.
Ikke kun kan gliomas arvet, men også sygdomme, der ledsages af øget tumorvækst uden henvisning til lokaliseringen-især kan dette være neurofibromatosis type 1 og 2, Li-Fraumeni syndrom, Hippel-Lindau. Ofte i gliomaceller detekteres ændringer i visse gener eller kromosomer.
De vigtigste patologier, der er forbundet med udviklingen af glioma hos mennesker, er sammenfattet i tabellen:
Patologi |
Kromosom |
Gen |
Mangfoldighed af neoplasma |
Li-Fraumeni syndrom |
17р13 |
TR53 |
Neuroektodermale neoplasmer, astrocytom. |
Neurofibromatose |
17Q11 |
NF1 |
Optisk nerv gliom, pilocytisk astrocytom, neurofibromatose |
Turcottes syndrom |
3p21, 7p22 |
HMLH1, HPSM2 |
Astrocytoma |
Tuberøs sklerose (Burnevilles syndrom). |
9q34, 16p13 |
Tsc1, tsc2 |
Gigantocellulært subafhængig astrocytom |
Uanset arten af glialtumoren, hvad enten det er en sporadisk sag eller en arvelig patologi, er det en lidelse med ekspressionen af et patologisk ændret gen. Bortset fra neoplasmer dannet som et resultat af læringseffekter, er årsagerne til genetiske ændringer i andre situationer uklare.
Symptomer Hjernegliomer
Funktioner ved fokal symptomatologi afhænger direkte af området med lokalisering af hjerne glioma og bliver en konsekvens af alle slags endokrine lidelser, komprimering af nervevæv eller lokale destruktive processer.
Hvis neoplasmaet er placeret i parietalzonen, domineres en person af manifestationer som anfald, sensoriske lidelser, hørselsnedsættelse.
Når glioma er lokaliseret i området med den dominerende halvkugle, opdages taleforstyrrelser, agraphia, agnosia.
Temporale lobeoplasmer ledsages ofte af krampagtige anfald, afasi, nedsat lugtesans og visuel funktion og dyspnø.
Når det intrakranielle tryk øges, udvikles et tilsvarende billede med begrænsning af synsfelter, lammelse af øjenmuskler og hemiplegi.
På grund af specificiteten af tumorprocessen ledsages hjerne glioma altid af neurologiske symptomer i større eller mindre grad. Først er der en mærkbar generel svaghed, patienten ønsker konstant at sove, evnen til arbejde er nedsat, tankeprocesser bremses. Det er på dette tidspunkt, at der er en høj risiko for at stille en forkert diagnose og som en konsekvens heraf ordinerer den forkerte behandling. Blandt andre ikke-specifikke manifestationer:
- Vestibulære lidelser, herunder ustabil gang, tab af balance (f.eks. Når cykling eller klatre trapper), følelsesløshed i lemmerne osv.;
- Gradvis forringelse af synet, fordobling af det visuelle billede;
- Forringelse af auditiv funktion;
- Sløret tale;
- Kvalme og opkast i form af angreb uafhængigt af mad eller drikke;
- Svækkelse af efterligningsmusklerne og andre ansigtsmuskler;
- Ubehag, når man sluger;
- Regelmæssig hovedpine (ofte i morgentimerne).
Det kliniske billede udvides gradvist og forværres: hos nogle patienter sker det langsomt, i andre - pludselig, bogstaveligt talt "for deres øjne" inden for et par uger. I sidstnævnte tilfælde taler vi om en aggressiv, hurtigt udviklende gliom i hjernen.
Første tegn
Glioma i hjernen i de tidlige udviklingsstadier har ikke en udtalt symptomatologi. De første manifestationer forveksles ofte med tegn på andre, mindre farlige patologier.
Generelt er det kliniske billede af glioma forskelligartet og bestemmes af placeringen og størrelsen af det patologiske fokus. Efterhånden som neoplasmaet vokser, udvikler og øges generelle cerebrale symptomer:
- Vedvarende og regelmæssige hovedsmerter, der ikke reagerer på standardmedicin (ikke-steroide antiinflammatoriske lægemidler);
- Intermitterende kvalme, undertiden til opkast;
- En ubehagelig, tung følelse i øjeæbleområdet;
- Anfald.
Cerebrale manifestationer er især intense, når tumoren vokser ind i ventriklerne eller spiritussystemet. Cerebrospinalvæskedrenering er nedsat, det intrakranielle tryk øges, og hydrocephalus udvikler sig. Processen påvirker en bestemt del af hjernen, der påvirker udviklingen af den tilsvarende klinik:
- Der er problemer med visuel funktion;
- Tale nedsat;
- Vestibulære lidelser (svimmelhed, nedsat koordinering af bevægelser) forekommer;
- Parese, lammelse af armene, benene;
- Hukommelse og koncentration er nedsat;
- Tankeprocesser er nedsat;
- Adfærdsforstyrrelser dukker op.
På det indledende trin er symptomerne praktisk talt fraværende, eller de er så ubetydelige, at de ikke tiltrækker opmærksomhed. Det er af denne grund, at eksperter stærkt rådgiver regelmæssige forebyggende undersøgelser og kontrol. Når alt kommer til alt, jo tidligere tumorprocessen detekteres, jo større er chancerne for kur og overlevelse. [5]
Glioma i hjernen hos et barn
Blandt de mange hjernesvulster, der findes i barndommen, varierer procentdelen af gliomas fra 15 til 25%. Børn kan få sygdommen i deres tidlige teenagere og tidlige tyverne, selvom det er meget sjældent for babyer under 3 år at få sygdommen.
Patologien starter på baggrund af mutation af gliaceller. Til dato er der ikke noget svar på spørgsmålet om, hvorfor denne mutation opstår.
Det eneste, der er blevet pålideligt lært, er, at visse arvelige sygdomme, der er forbundet med en øget risiko for tumorvækst, øger sandsynligheden for at udvikle hjerne glioma også.
Derudover har forskere fundet, at glialceller kan have divergens i individuelle gener eller kromosomer. På grund af denne lidelse sparker en mutationsmekanisme ind, som ikke er arvelig. Det er muligt, at dette sker på et af de tidligste udviklingsstadier.
Det er en bevist kendsgerning, at tilstedeværelsen af akut leukæmi eller retinoblastom i barnets historie eller hjernebestråling af anden grund markant øger risikoen for dannelse af gliom (efter en bestemt periode).
Symptomatologi i barndommen afhænger af graden af malignitet og lokalisering af det patologiske fokus. Der sondres mellem specifikke og ikke-specifikke symptomer:
- Ikke-specifikke symptomer er ikke "bundet" til det område, hvor gliomet er placeret. Almindelige manifestationer kan omfatte hovedsmerter, svimmelhed, dårlig appetit, opkast uden forbindelse med madindtagelse, vægttab (af ukendte årsager), konstant følelse af træthed, fald i akademisk præstation, vanskeligheder i koncentration, adfærdsforstyrrelser. Disse tegn skyldes komprimering af intrakranielle strukturer, som kan forklares som et direkte tryk af den voksende masse og en lidelse i cirkulationen af cerebrospinalvæske. Der er risiko for cerebral hydrocele.
- Den specifikke symptomatologi afhænger af den øjeblikkelige placering af det gliale patologiske fokus. For eksempel ledsages cerebellar tumor normalt af nedsat gang og balance hos børn. Læsionen i den store hjerne manifesteres ved krampagtige anfald og tumorvækst i rygmarven - lammelse af muskulaturen. Det sker, at babyens vision forværres skarpt, bevidstheden forstyrres, søvn er nedsat, eller der opstår et andet udviklingsproblem.
Som regel afslører ondartet glioma i barndommen sig selv om et par uger eller måneder af dens udvikling: ofte kendetegnet ved hurtig og ukontrolleret vækst af neoplasmaet.
Børn med ondartede glialtumorer behandles af læger på pædiatriske kliniske centre, der specialiserer sig i pædiatrisk onkologi. Som regel anvendes kirurgisk behandling, stråling og kemoterapikurser.
Det vigtigste behandlingstrin er neurokirurgi. Jo mere radikal det er, jo bedre er barnets chancer for en kur. Men kirurgisk indgreb er ikke altid mulig: Især kan der opstå problemer med fjernelse af hjernestammens gliomas såvel som med stråling for børn under 3 år.
Gliomas i den centrale hjerne (mellemliggende og mellemhjernen) er vanskelige at fjerne fuldstændigt, da der er risiko for skade på sundt væv. Hvis fuldstændig resektion af tumoren er umulig, ordineres patienten palliativ behandling.
Børn med ondartede gliomas behandles i henhold til standardiserede protokoller, der er blevet bestemt gennem strengt kontrollerede kliniske forsøg. De mest almindelige protokoller er som følger:
- Hit HGG 2007: involverer behandling af børn i alderen 3-17 år.
- Hit SKK: Velegnet til spædbørn (op til tre år) og involverer ikke strålebehandlinger.
Pædiatrisk overlevelsesstatistik for gliomas er generelt ikke særlig optimistiske. Imidlertid er det imidlertid muligt på forhånd at forudsige effektiviteten af behandlingsforanstaltninger for et bestemt barn. Det er vigtigt at følge alle lægens ordrer omhyggeligt, hvilket markant øger chancerne for bedring.
Forms
Gliomas kan være lav malign og høj malign, med intens vækst og en tilbøjelighed til at metastasere. Det er vigtigt at forstå, at lav malignitet ikke er synonymt med tumorsikkerhed. Enhver hjerne-neoplasma skaber yderligere volumen, klemmer hjernestrukturer, hvilket fører til deres forskydning og øget intrakranielt tryk. Som et resultat kan patienten dø.
Der er to hovedtyper af ondartede astrocytomer. Dette er glioblastomer og anaplastiske astrocytomer, som er opdelt i henhold til molekylære ændringer. Sekundære ondartede tumorer, der udviklede sig fra astrocytomer og har en lav grad af malignitet, findes oftest hos unge patienter. Oprindeligt forekommer ondartede glial-type tumorer oftere hos ældre patienter.
Afhængig af den strukturelle placering kommer gliomas ind:
- Supratentorial (med lokalisering over cerebellum i området med laterale ventrikler, store halvkugler);
- Subtentorial (med lokalisering under cerebellum i den bageste kraniale fossa).
I henhold til histologiske træk skal du skelne sådanne typer gliomas:
- Astrocytisk gliom er det mest almindelige. Til gengæld er det opdelt i nodulær og diffus (sidstnævnte kan karakteriseres ved hurtig vækst og et slagmønster).
- Oligodendroglioma - forekommer hos 5% af patienterne. Det har petrificater - forkalkningsområder, oftest i frontalben.
- Ependymal glioma - vokser fra strukturer, der forer væggene i den centrale kanal i rygmarven og ventriklerne. Vokser ofte til tykkelsen af hjernestoffet såvel som til hjernens lumen.
Blandede patologiske foci såsom underafhængighed, oligoastrocytom osv. Er også mulige.
Alle gliomas er kategoriseret i de følgende faser:
- Langsom voksende relativt godartede neoplasmer uden åbenlyse kliniske symptomer.
- Langsomt voksende "grænse" gliomas, der gradvist omdannes til fase III og videre.
- Ondartet gliom.
- Ondartet gliom med intens aggressiv vækst og spredning med dårlig prognose.
Jo lavere scenen med malignitet, jo mindre sandsynlighed for metastase og gentagelse af den fjernede neoplasma, og jo større er chancerne for hærdning for patienten. Den største fare udgør af glioblastoma multiforme, en lavdifferentieret proces med intensiv vækst og udvikling. [6]
Mulige og mest almindelige varianter af neurogliom:
- Glioma med hjernestamme og pontin-læsioner er placeret i det område, hvor hjernen forbinder til rygmarven. Det er der, at vigtige neurocenter, der er ansvarlige for respiratorisk, hjerte- og motorisk funktion, er lokaliseret. Hvis denne zone er beskadiget, forstyrres det vestibulære og taleapparats arbejde. Det opdages ofte i barndommen.
- Visuelt gliom påvirker neurogliale celler, der omgiver synsnerven. Patologien forårsager synshandicap og exophthalmos. Det udvikler sig oftere hos børn.
- Lavt ondartet neurogliom er kendetegnet ved langsom vækst, lokaliseret oftere i de store halvkugler og cerebellum. Det forekommer oftere hos unge (unge og unge voksne omkring 20 år).
- Glioma i corpus callosum er mere karakteristisk for individer mellem 40 og 60 år og er oftest repræsenteret af glioblastoma.
- Glioma i Chiasma er lokaliseret i den optiske krydszone, så det ledsages af nærsynethed, tab af synsfelt, okklusiv hydrocephalus og neuroendokrine lidelser. Det kan forekomme i alle aldre, men påvirker oftest patienter med neurofibromatosis type I.
Komplikationer og konsekvenser
Gliomas af lav malignitet (grad I-II, meget ondartet - f.eks. Astrocytom, oligoastrocytom, oligodendroglioma, pleomorf xanthoastrocytoma osv.) Og høj malignitet (grad III-IV - glioblastoma, anaplastisk oligodendroglioma, oligoastrocytoma, And Andet, ANDAGLASTOMA Astrocytoma). Grad IV gliomas er især ondartede.
Hjernestamme glioma har en meget ugunstig prognose netop fordi neoplasmaet påvirker en sådan hjerneområde, hvor de vigtigste nervesammenhæng mellem hjernen og lemmerne er koncentreret. Selv en temmelig lille tumor i dette område er nok til at gøre patientens tilstand hurtigt forværres og provokerer lammelse.
Ikke mindre ugunstige konsekvenser opstår, når andre hjerneområder påvirkes. Ofte er det en tumor af cerebral cortex, som ikke giver en chance for en lang forventet levetid for patienten på trods af behandlingen. Det er ofte kun muligt at udsætte døden.
I henhold til medicinsk statistik er den femårige overlevelsesrate ofte kun 10-20%. Selvom disse tal stort set afhænger af både maligniteten og den nøjagtige lokalisering og volumen af kirurgisk intervention udført. Efter fuldstændig fjernelse af det patologiske fokus øges overlevelsesraten markant (undertiden - op til 50%). Manglende behandling eller dens umulighed (af en eller anden grund) er garanteret at føre til patientens død.
Størstedelen af lave maligne glialtumorer er i stand til at infiltrere hjernevæv og malignere over flere år.
Risikoen for tilbagefald af glioma betragtes af eksperter som "meget sandsynlige". Ikke desto mindre bør behandling ikke overses: det er vigtigt at sikre en god livskvalitet så længe som muligt.
Tilbagevendende gliomas har altid en værre prognose end primære tumorer. Imidlertid opnår moderne behandlingsprotokoller baseret på terapeutiske optimeringsundersøgelser ofte tilstrækkeligt gode resultater for patienter, selv med meget ondartede neoplasmer.
Mulige resultater efter kemoterapi:
- Afmagring, afmagring, fordøjelsesforstyrrelser, orale sygdomme;
- Øget excitabilitet af det centrale nervesystem, astheni;
- Forringelse af hørelsesfunktion, tinnitus og ring i ørerne;
- Anfald, depressive lidelser;
- Hypertensiv krise, ændring i blodmønster;
- Nyresvigt;
- Allergiske processer, hårtab, udseende af pigmentpletter på kroppen.
Efter kemoterapi bemærker patienterne en markant svækkelse af immunsystemet, hvilket kan forårsage udvikling af forskellige infektiøse patologier.
Diagnosticering Hjernegliomer
En hjerne gliom kan mistænkes af følgende tegn:
- Patienten har lokaliseret eller generaliserede anfald, som er karakteristiske for den kortikale placering af neoplasmaet og dens langsomme udvikling. EPI-syngene findes hos 80% af patienterne med glialtumorer med lav kvalitet og hos 30% af patienter med høj kvalitet gliomas.
- Øget intrakranielt tryk er især karakteristisk for masser placeret i de højre frontale og parietale lober. Forbundet med høj intrakranielt trykforstyrrelse i blodcirkulation og spirituscirkulation indebærer udseendet af konstant og stigende hovedsmerter, kvalme med opkast, synsforstyrrelser, døsighed. Der er ødemer af synsnerven, lammelse af afledningsnerven. En stigning i intrakranielt pres på kritiske værdier kan føre til udvikling af koma og død. En anden årsag til høj IOP er hydrocephalus.
- Patienten har et voksende fokalt billede. I supratentoriale formationer forstyrres de motoriske og sensoriske kugler, hæmiopi, afasi og kognitive lidelser.
Hvis lægen har mistanke om tilstedeværelsen af en hjernens neoplasma, er det optimalt at udføre MR uden eller med introduktionen af kontrastmiddel (gadolinium) for at finde ud af dens placering, størrelse og yderligere egenskaber. Hvis magnetisk resonansafbildning ikke er mulig, udføres computertomografi, og magnetisk resonansspektroskopi anvendes som en metode til differentiering. På trods af informativiteten af disse diagnostiske metoder stilles den endelige diagnose først efter histologisk bekræftelse under resektion af tumorfokus.
I betragtning af ovenstående kriterier anbefales det at begynde diagnose med en grundig historie, vurdering af somato-neurologisk status og funktionel status. Neurologisk status vurderes sammen med bestemmelsen af sandsynlige intellektuelle og mnestiske lidelser.
Anbefalede laboratorieundersøgelser:
- En fuldblæst klinisk blodoparbejdning;
- Et panel med fuld blodkemi;
- Urinalyse;
- Blodkoagulationsundersøgelse;
- Analyse for onkologiske markører (AFP, beta-HCG, LDH - relevant, hvis der er mistanke om en læsion i pinealzonen).
For at afklare prognostiske punkter hos patienter med glioblastoma og anaplastisk astrocytoma evalueres IDH1 | 2-1 genmutation og Mgmt-genmethylering. Hos patienter med oligodendroglioma og oligoastrocytoma bestemmes 1p | 19q-kodelering.
Instrumental diagnostik er først og fremmest repræsenteret ved obligatorisk magnetisk resonansafbildning af hjernen (undertiden - og rygmarv). MR udføres i tre fremskrivninger ved anvendelse af standard T1-2, Flair, T1-tilstande med kontrast.
Når den er indikeret, ultralyd af det vaskulære netværk, udføres funktionel magnetisk resonansafbildning af motor- og talesektioner samt angiografi, spektroskopi, hr. Traktografi og perfusion.
Yderligere undersøgelser kan omfatte:
- Elektroencefalografi af hjernen;
- Konsultationer med en neurokirurg, onkolog, radiolog, øjenlæge, radiolog.
Differential diagnose
Differentialdiagnose udføres nødvendigvis med ikke-tumorpatologier-især med blødning forårsaget af arterio-venøs eller arteriel misdannelse såvel som med pseudotumor demyeliniserende processer, inflammatoriske sygdomme (toxoplasmosis, hjerneabcess osv.).
Derudover differentierer det primære tumorfokus og metastaser i centralnervesystemet.
Med moderne magnetisk resonansafbildningskapacitet er det muligt at udføre diagnostiske foranstaltninger nøjagtigt nok for at finde ud af oprindelsen af det primære fokus i CNS. MR af hjernen udføres med eller uden kontrast, i T1, T2 flair-tilstand - i tre fremskrivninger eller tynde skiver i aksial projektion (SPGR-tilstand). Disse diagnostiske metoder giver mulighed for nøjagtigt at bestemme placering, størrelse, strukturelle egenskaber ved neoplasmaet, dets forhold til det vaskulære netværk og hjerneområder i nærheden.
Derudover kan CT (med eller uden kontrast), CT-angiografi (Hr. Angiografi), Hr. Traktografi, MR eller CT-perfusion udføres som en del af den differentielle diagnose. CT/PET i hjernen med methionin, cholin, tyrosin og andre aminosyrer anvendes, når det er indikeret.
Behandling Hjernegliomer
Specifik terapi består af kirurgiske, kemoterapeutiske og strålingsforanstaltninger. Det er om muligt obligatorisk at udføre en komplet resektion af tumorfokus, som muliggør hurtig symptomlindring og histologisk bekræftelse af diagnosen.
Bestråling har en positiv effekt på at øge patienternes levealder. En samlet dosis på 58 til 60 Gy, opdelt i individuelle bestrålingsdoser på 1,8-2 Gy, administreres som standard. Tumoren bestråles lokalt og fanger desuden op til 3 cm omkring den. Strålebehandling er mere acceptabel i modsætning til brachyterapi. I nogle tilfælde anbefales radiokirurgiske metoder, der består af bestråling med en gamma-kniv eller lineær gaspedal samt neutronfangstborterapi.
Behovet for adjuvans kemoterapi er kontroversielt. I nogle tilfælde tilladte Nitrosourea-præparater at øge de forventede levealder for patienter op til halvandet år, men nogle resultater af at bruge sådanne kemopreparationer var negative. I dag er cytotoksiske midler, neoadjuvant terapi (før stråling), kombinerede lægemidler, intra-arteriel kemoterapi eller højdosis kemoterapi med yderligere stamcelletransplantation aktivt anvendt.
Generelt for en vellykket behandling af gliomas er en omfattende tilgang meget vigtig, hvis omfang afhænger af placeringen og graden af malignitet i massen, dens størrelse og patientens generelle helbred.
I relation til hjernestamme glioma anvendes kirurgisk intervention sjældent. Den vigtigste kontraindikation til kirurgi er lokaliseringsområdet - i nærheden af vigtige dele. I nogle tilfælde er det muligt at fjerne glioma i bagagerummet ved hjælp af mikrosurgiske metoder med præoperativ og postoperativ kemoterapi. En sådan indgriben er meget kompleks og kræver særlige kvalifikationer af en neurokirurg.
Strålingskirurgi og især stereotaktisk kirurgi med eksponering for høje ioniserende doser er ret effektiv. Brugen af en sådan teknik i tidlige stadier af neoplasmaudvikling tillader undertiden at opnå langvarig remission eller endda fuldstændig helbredelse af patienten.
Stråling kombineres ofte med kemoterapi, hvilket forbedrer effektiviteten af interventioner og reducerer strålingsbyrden. I gliomas er ikke alle kemopreventive midler terapeutisk vellykkede, så de ordineres individuelt, og recept er justeret om nødvendigt.
For at reducere smerter og lavere intrakranielt tryk, uanset den vigtigste behandling, ordineres symptomatisk terapi - især kortikosteroidlægemidler, smertestillende midler, beroligende midler.
Medicin
Kortikosteroidlægemidler påvirker hævelse, reducerer sværhedsgraden af neurologiske symptomer i flere dage. På grund af flere bivirkninger og øget sandsynlighed for ugunstige interaktioner med kemoterapimedicin anvendes imidlertid minimalt effektive doser af steroider, hvilket afbryder dem så hurtigt som muligt (f.eks. Efter operationen).
Antikonvulsiva anvendes systematisk som en sekundær forebyggende foranstaltning hos patienter, der allerede har oplevet epileptiske anfald. Disse medicin kan forårsage alvorlige bivirkninger og også interagere med kemoterapimedicin.
Antikoagulantia er især relevante på det postoperative stadium, da risikoen for thrombophlebitis-dannelse i glioma er ret høje (op til 25%).
En god effekt forventes ved at tage antidepressiv-angreb. Brugen af methylphenidat 10-30 mg/dag i to doser gør det ofte muligt at optimere kognitive evner, forbedre livskvaliteten, opretholde arbejdsevnen.
Neurologisk svigt og tegn på cerebralt ødem (smerter i hovedet, forstyrrelser i bevidsthed) elimineres af kortikosteroidlægemidler - især prednisolon eller dexamethason. |
Skemaet og doseringen af kortikosteroider vælges individuelt med praksis med den minimale effektive dosis. Ved afslutningen af behandlingsforløbet trækkes lægemidlerne gradvist tilbage. |
Kortikosteroider er sammen med gastrobeskyttende lægemidler-protonpumpeblokkere eller H2-histaminBlokkere. |
Diuretika (furosemid, mannitol) er ordineret til svær hævelse og forskydning af hjernestrukturer som et supplement til kortikosteroidlægemidler. |
I tilfælde af krampagtige anfald (inklusive anamnesis) eller epileptiforme symptomer på elektroencefalogram er antikonvulsant terapi yderligere ordineret. Anticonvulsiva er ikke ordineret til profylaktiske formål. |
Patienter med indikationer for kemoterapi anbefales at tage antikonvulsiva, der ikke påvirker leverenzymfunktionen. Valg af medikamenter: Lamotrigin, Valproinsyre, levetiracetam. Bør ikke bruges: Carbamazepin, phenobarbital. |
Hovedsmerter i hjerne gliomas styres med kortikosteroidbehandling. |
I nogle tilfælde af hovedpine kan ikke-steroide antiinflammatoriske lægemidler eller tramadol anvendes. |
Hvis patienten tager ikke-steroide antiinflammatoriske lægemidler, afbrydes de et par dage før operationen for at minimere chancen for blødning under operationen. |
I valgte smerter i smerter kan narkotiske smertestillende midler - såsom fentanyl eller trimeperidin - anbefales. |
For at forhindre lungeemboli fra den tredje postoperative dag, er administration af hepariner med lav molekylvægt - især enoxaparin-natrium eller nadroparin-calcium - ordineret. |
Hvis patienten er på systematisk antikoagulant- eller antiaggregant behandling, overføres han til lavmolekylvægthepariner senest en uge før kirurgisk intervention, med deres yderligere tilbagetrækning en dag før operation og genoptagelse 24-48 timer efter operationen. |
Hvis en patient med glioma har venøs trombose i de nedre ekstremiteter, udføres behandling med direkte antikoagulantia. Muligheden for at placere et Cava-filter er ikke udelukket. |
Kemoterapi til maligne gliomas i hjernen
De grundlæggende antitumorkemoterapiregimer for gliomas anses for at være:
- Lomustine 100 mg/m² på første dag, Vincristine 1,5 mg/m² på dage og otte, procarbazin 70 mg/m² fra dag otte til 21 år, kurser hver sjette uge.
- Lomustine 110 mg/m² hver sjette uge.
- Temozolomide 5/23 150 til 200 mg/m² fra dag en til dag fem, hver 28. dag.
- Temozolomid som en del af kemoradieringsbehandling, 75 mg/m² hver dag, der gives stråling.
- Temozolomid med cisplatin eller carboplatin (80 mg/m²) og temozolomid 150-200 mg/m² på dag 1 til 5 hver 4. uge.
- Temozolomide 7/7 ved 100 mg/m² på dag 1-8 og 15-22 af kurset med en gentagelse hver fjerde uge.
- Bevacizumab 5 til 10 mg/kg på dage én og femten, og irinotecan 200 mg/m² på dage 1 og femten, gentaget hver fjerde uge.
- Bevacizumab 5 til 10 mg/kg på dage 1, femten og niogtyve og Lomustine 90 mg/m² på dag ét hver sjette uge.
- Bevacizumab 5 til 10 mg/kg på dage én og femten, Lomustine 40 mg på første, otte, femten og toogtyve, gentaget hver sjette uge.
- Bevacizumab 5 til 10 mg/kg på dag 1 og femten, gentaget hver fjerde uge.
Cytostatiske lægemidler hæmmer i mange tilfælde med succes væksten af tumorceller, men viser ikke selektivitet over for sunde væv og organer. Derfor har eksperter identificeret en række kontraindikationer, hvor kemoterapi af gliom er umulig:
- Overdreven individuel følsomhed over for kemopreventive midler;
- Nedbrydning af hjerte, nyre, leverfunktion;
- Deprimeret hæmatopoiesis i knoglemarven;
- Problemer med binyrefunktion.
Kemoterapi administreres med ekstrem forsigtighed:
- Patienter med betydelige hjerterytmeforstyrrelser;
- Med diabetes;
- Til akutte virusinfektioner;
- Til ældre patienter;
- Patienter, der lider af kronisk alkoholisme (kronisk alkoholforgiftning).
Den mest alvorlige bivirkning af kemopreventive lægemidler er deres toksicitet: cytostatik forstyrrer selektivt funktionaliteten af blodlegemer og ændrer deres sammensætning. Som en konsekvens falder blodplade- og erytrocyttemasse, og anæmi udvikler sig.
Før lægen ordinerer en patient et kursus med kemoterapi, tager lægen altid højde for graden af toksicitet af lægemidlerne og de sandsynlige komplikationer efter deres anvendelse. Kemoterapikurser overvåges altid omhyggeligt af specialister og regelmæssig blodovervågning.
Mulige konsekvenser af cytostatisk terapi:
- Gauntness, afmagring;
- Sværhedsgrad med at sluge mad, tørre slimhinder, periodontitis, dyspepsi;
- Instabilitet i centralnervesystemet, manisk-depressive lidelser, anfaldssyndrom, astheni;
- Forringelse af auditiv funktion;
- Stigning i blodtrykket op til udviklingen af hypertensiv krise;
- Fald i blodplader, røde blodlegemer, hvide blodlegemer, flere blødninger, intern og ekstern blødning;
- Nyresvigt;
- Allergiske processer;
- Hårtab, udseendet af områder med øget pigmentering.
Efter kemoterapikurser har patienter en øget risiko for at udvikle infektionssygdomme, og muskel- og ledssmerter er almindelig.
For at reducere risikoen for ugunstige post-kemoterapeutiske effekter er der nødvendigvis foreskrevet yderligere rehabiliteringsforanstaltninger, hvis formål er at gendanne normalt blodantal, stabilisering af hjerte-kar-aktivitet, normalisering af neurologisk status. Der udøves nødvendigvis tilstrækkelig psykologisk støtte.
Kirurgisk behandling
Operationen udføres for at fjerne tumorfokus så meget som muligt, hvilket igen skal reducere det intrakranielle tryk, reducere neurologisk insufficiens og tilvejebringe det nødvendige biomateriale til forskning.
- Operationen udføres i en specialiseret neurokirurgisk afdeling eller klinik, hvis specialister opleves i neuro-onkologiske interventioner.
- Kirurgen udfører adgang ved plastikknoglegering inden for den mistænkte glioma-lokalisering.
- Hvis neoplasmaet er placeret anatomisk tæt på motoriske områder eller veje eller i kernerne eller langs kraniale nerver, anvendes intraoperativ neurofysiologisk overvågning.
- Neuronavigationssystemer, intraoperativ fluorescensnavigation med 5-aminolevuleninsyre er ønskelig for at maksimere fjernelse af neoplasmaet.
- Efter interventionen udføres en kontrol CT eller MR (med eller uden kontrastinjektion) på dag 1-2.
Hvis kirurgisk resektion af glioma er umulig eller oprindeligt anerkendt som uønsket, eller hvis der er mistanke om lymfom i centralnervesystemet, udføres en biopsi (åben, stereotaktisk, med navigationsovervågning osv.). |
Patienter med cerebral gliomatose verificeres ved stereotaktisk biopsi, da terapeutisk taktik stort set afhænger af det histologiske billede. |
I visse situationer - hos ældre patienter, i tilfælde af alvorlige neurologiske lidelser, er det i tilfælde af lokalisering af gliom i bagagerummet og andre vitale dele planlagt baseret på symptomer og billeddannelsesinformation efter en generel medicinsk konsultation. |
Patienter med piloid astrocytom såvel som nodulære former for hjernestamme neoplasmer og eksofytiske processer anbefales at gennemgå resektion eller åben biopsi. |
Patienter med diffus pontin glioma og andre diffuse neoplasmer af bagagerummet behandles med stråling og antitumorlægemiddelbehandling. Verifikation er ikke nødvendig i sådanne tilfælde. |
Patienter med quadriplegisk plade glioma gennemgår systematisk magnetisk resonans og klinisk overvågning efter fjernelse af cerebral hydrocele. Hvis neoplasmaet viser tegn på vækst, fjernes den med yderligere bestråling. |
Når delvis resektion eller biopsi af en malign glioma med lav kvalitet udføres, behandles patienter med to eller flere risikofaktorer nødvendigvis med stråling og/eller kemoterapi. |
Total resektion er obligatorisk for patienter med subafhængig gigantcelle-astrocytom. |
Everolimus er ordineret til diffus subafhængig gigantcelle-astrocytom. |
Piloid astrocytom skal fjernes med magnetisk resonansafbildning efter intervention for at afklare kvaliteten af radikal resektion af tumorvæv. |
I glioblastoma skal postoperativ terapi kombineres (stråling + kemoterapi) med temozolomidadministration. |
I anaplastisk astrocytom efter operation er strålebehandling med yderligere lægemiddelterapi indikeret. Lomustine, temozolomid anvendes. |
Patienter med anaplastisk oligodendrogliom eller oligoastrocytom får både stråling og kemoterapi (temozolomid eller PCV monoterapi) efter operationen. |
Ældre patienter med omfattende høj malign glioma bestråles i hypofraktioneret tilstand, eller monoterapi med temozolomid udføres. |
I tilfælde af gliom-gentagelse diskuteres muligheden for reoperation og efterfølgende behandlingstaktikker af et konsilium af specialister. Det optimale regime for gentagelser: Reoperation + systemisk kemoterapi + gentagen strålingseksponering + palliative mål. Hvis der er lokaliserede mindre områder med tilbagevendende tumorvækst, kan radiokirurgi anvendes. |
De valgte lægemidler til tilbagevendende gliomvækst er temozolomid og bevacizumab. |
Gentagelse af meget ondartede oligodendrogliomas og anaplastiske astrocytomer er en indikation for temozolomidbehandling. |
Pleomorf Xanthoastrocytoma fjernes uden obligatorisk adjuvans kemoterapi. |
En af de særegenheder ved gliomas er vanskeligheden ved deres behandling og fjernelse. Kirurgen sigter mod at fjerne vævene i neoplasmaet så fuldstændigt som muligt for at opnå kompensation af tilstanden. Mange patienter er i stand til at forbedre livskvaliteten og forlænge den, men for meget ondartede tumorer forbliver prognosen ugunstig: der er en øget sandsynlighed for genvækst af det patologiske fokus.
Ernæring til glioma i hjernen
Diæt til patienter med ondartede tumorer - et vigtigt punkt, som mange mennesker desværre ikke er meget opmærksomme på. I mellemtiden, takket være ændringer i diæt, er det muligt at bremse udviklingen af gliom og styrke og rystet immunitet.
Store områder med diætændring:
- Normalisering af metaboliske processer, styrkelse af immunbeskyttelse;
- Afgiftning af kroppen;
- Optimering af energipotentiale;
- At sikre normal funktion af alle organer og systemer i kroppen i en så vanskelig periode for dem.
Rationel og afbalanceret diæt er nødvendig, da patienter med tidlige stadier af lave maligne neoplasmer og patienter med den sidste fase af glioblastoma. Omhyggeligt udvalgt diæt bidrager til forbedring af generel velvære, bedring af beskadigede væv, hvilket er især vigtigt på baggrund af cytostatisk og strålebehandling. Balancen mellem ernæringskomponenter og korrekte metaboliske processer forhindrer dannelse af infektiøse foci, blokerer inflammatoriske reaktioner, forhindrer udmattelse af kroppen.
Følgende fødevarer og drikkevarer anbefales til hjerne gliom:
- Røde, gule og orange farvede frugter og grøntsager (tomater, ferskner, abrikoser, gulerødder, rødbeder, citrusfrugter) indeholdende carotenoider, der beskytter sunde celler mod de negative virkninger af strålebehandling;
- Kål (blomkål, broccoli, rosenkål), radise, sennep og andre planteprodukter, der indeholder indol - et aktivt stof, der neutraliserer ugunstige giftige og kemiske faktorer;
- Grønne (dild, persille, unge mælkebøtter og brændenælde blade, rabarber, ruccola, spinat), grønne ærter og asparges, asparges bønner og alger (tang, spirulina, chlorella);
- Grøn te;
- Hvidløg, løg, ananas, der har antitumor- og afgiftningsevne;
- Bran, korn, fuldkornsbrød, spirede spirer med bælgfrugter, korn og frø;
- Mørke druer, hindbær, jordbær og jordbær, blåbær, brombær, granatæble, rips, sortkurranter, rowanberries, blåbær, havtorn, kirsebær og andre bær, der indeholder naturlige antioxidanter, der reducerer de negative virkninger af frie radikaler, vira og carcinogens;
- Mejeriprodukter med lavt fedtindhold.
Du bør ikke belaste fordøjelsessystemet og hele kroppen med tunge og fedtholdige fødevarer. Det er nyttigt at bruge friskpresset hjemmelavede juice, smoothies, stammel. Kilder til omega-3-fedtsyrer, såsom fiskeolie, hørfrøolie eller hørfrø, skal tilsættes til retter.
Det er bedre at undgå sukker og slik helt. Men en skefuld honning med en kop vand vil ikke skade: Bee-produkter har en udtalt antiinflammatorisk, antioxidant og antitumoreffekt. Den eneste kontraindikation til brugen af honning er en allergi over for produktet.
Fra kosten skal udelukkes:
- Kød, smult, slagteaffald;
- Smør, fedtmejeriprodukter;
- Røget kød, pølser, dåse kød og fisk;
- Alkohol i enhver form;
- Slik, kager, kager og kager, slik og chokolade;
- Bekvemmelighedsfødevarer, fastfood, snacks;
- Stegt mad.
Du skal forbruge nok grøntsager, greener, frugter og rent drikkevand på daglig basis.
Under kemoterapi og i nogen tid efter det skal du drikke hjemmelavet grøntsags- og frugtsaft, spise hjemmelavet fedtfattigt cottage cheese, mælk og ost. Det er vigtigt at drikke masser af væsker, børste dine tænder og skylle munden ofte (ca. 4 gange om dagen).
Optimale måltider til hjernens gliomapatienter:
- Vegetabilske gryderetter;
- Side retter og supper lavet af korn (fortrinsvis boghvede, havregryn, ris, couscous, bulgur);
- Dampede ostekager, buddinger, gryderetter;
- Stuede og bagt grøntsager;
- Gryderetter, grøntsagssupper, første og anden retter fra bælgfrugter (inklusive soja), pâtés og soufflés;
- Smoothies, grøn te, kombinerer og stumler.
Forebyggelse
Hvis en person fører en sund livsstil, og blandt sine pårørende var der ingen tilfælde af kræftpatologi, har han enhver chance for ikke at få hjernes gliom. Der er ingen specifik forebyggelse af sådanne tumorer, så de vigtigste forebyggende punkter anses for at være korrekt ernæring, fysisk aktivitet, undgåelse af dårlige vaner, fravær af erhvervsmæssige og husholdningsfarer.
Specialister giver en række enkle, men alligevel effektive anbefalinger:
- Drik mere rent vand, undgå sødede sodavand, pakket juice, energidrikke og alkohol.
- Undgå erhvervs- og husholdningsfarer: Mindre kontakt med kemikalier, ætsende løsninger og væsker.
- Prøv at tilberede mad ved at koge, stewing, bagning, men ikke stege. Giv præference for sunde hjemmelavede fødevarer.
- En stor del af din diæt skal være plantefødevarer, inklusive greener, uanset årstiden.
- En anden negativ faktor er at blive overvægtig, som skal slippes af med. Vægtkontrol er meget vigtig for helheden i hele kroppen.
- Vegetabilske olier skal altid foretrækkes frem for smør og smult.
- Hvis det er muligt, er det ønskeligt at foretrække miljøvenlige produkter, kød uden hormoner, grøntsager og frugter uden nitrater og pesticider. Det er bedre at undgå rødt kød helt.
- Tag ikke multivitaminpræparater uden indikationer og i store mængder. Tag ikke medicin uden en læges recept: Selvmedicinering er ofte meget, meget farlig.
- Hvis der opstår mistænkelige symptomer, er det nødvendigt at besøge en læge uden at vente på forværringen af situationen, udviklingen af bivirkninger og komplikationer.
- Slik og fødevarer med et højt glykæmisk indeks er en uønsket komponent i kosten.
- Jo tidligere en person går til lægerne, jo bedre er hans chancer for kur (og dette gælder for næsten enhver sygdom, inklusive glioma i hjernen).
For at forhindre dannelse af onkopatologi har du brug for nok tid til at sove og hvile, undgå overdreven forbrug af alkoholholdige drikkevarer, give præference for naturlig mad af høj kvalitet, reducere brugen af gadgets (især mobiltelefoner).
Tumorsygdomme forekommer ofte hos ældre og gamle mennesker. Derfor er det vigtigt at overvåge dit eget helbred fra en ung alder og ikke at provokere patologiske processer ved usunde livsstil og usunde vaner.
De nøjagtige rodårsager til onkologi er endnu ikke klaret. Imidlertid spiller en bestemt rolle naturligvis ugunstige erhvervsmæssige og miljømæssige forhold, eksponering for ioniserende og elektromagnetisk stråling, hormonelle ændringer. Bliv ikke lang og regelmæssigt under solen, lad pludselige ændringer i omgivelsestemperatur, overophedes i badet eller saunaen, ofte tage varme bade eller brusere.
Et andet spørgsmål: Hvordan kan man forhindre en gentagelse af hjerne gliom efter dens vellykkede behandling? Gentagelse af neoplasma-vækst er en kompleks og desværre hyppig komplikation, hvilket er vanskeligt at forudsige på forhånd. Patienter kan anbefales at gennemgå regelmæssige forebyggende undersøgelser og kontrol, besøge en onkolog og deltage i læge mindst to gange om året, føre en sund livsstil, spise sund og naturlig mad, praktisere moderat fysisk aktivitet. En anden tilstand er kærlighed til livet, sund optimisme, positiv holdning til succes under alle omstændigheder. Dette inkluderer også en venlig atmosfære i familien og på arbejde, tålmodighed og ubetinget støtte fra nære mennesker.
Vejrudsigt
Hjernens tilstand og egenskaberne ved glioma på tidspunktet for dets påvisning påvirker overlevelsesraten lige så meget som behandlingen, der administreres. En tilfredsstillende generel sundhed hos patienten og hans alder forbedrer prognosen (prognosen er mere optimistisk hos unge patienter). En vigtig indikator er det histologiske billede af neoplasmaet. Således har gliomas med lav kvalitet en bedre prognose end anaplastiske gliomas og endnu mere glioblastomas (de mest ugunstige tumorprocesser). Astrocytomer har en værre prognose end oligodendrogliomas.
Maligne astrocytomer reagerer dårligt på terapi og har en relativt lav overlevelsesrate på seks til fem år. På samme tid anslås forventet levealder i gliomas med lav kvalitet til 1-10 år.
Maligne astrocytomer er i det væsentlige uhelbredelige. Behandlingsretningen involverer normalt reduktion af neurologiske manifestationer (inklusive kognitiv dysfunktion) og øget forventet levealder, mens den højest mulige livskvalitet. Symptomatisk terapi tiltrækkes på baggrund af rehabiliteringsforanstaltninger. En psykologs arbejde er også vigtigt.
I løbet af det sidste årti har forskere gjort nogle fremskridt med at forstå arten af hjernesvulster og hvordan man behandler dem. Meget mere bør gøres for at optimere prognosen for sygdommen. Den primære opgave for specialister i dag er følgende: Brain Glioma skal have flere ordninger til effektiv eliminering af problemet på én gang, både i tidlige og efterfølgende udviklingsstadier.

