Medicinsk ekspert af artiklen
Nye publikationer
Leveramyloidose
Sidst revideret: 29.06.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Amyloidose er normalt en systemisk, generel patologi, der er karakteriseret ved ophobning af amyloid (et specifikt glykoprotein) i væv og efterfølgende forstyrrelse af normal organfunktion. Leveramyloidose er meget mindre almindelig end nyre og milt [ 1 ], men ledsager næsten altid systemisk skade på kroppen. Ingen af de eksisterende billeddannelsesteknikker kan specifikt påvise tilstedeværelsen af amyloid. Selv ved klinisk og radiologisk mistanke afhænger diagnosen amyloidose af vævsbiopsi for at bekræfte tilstedeværelsen af amyloidaflejringer. [ 3 ] Behandlingen er kompleks, omfattende og omfatter immunsuppressive og symptomatiske foranstaltninger. I alvorlige tilfælde kan levertransplantation være nødvendig.
Epidemiologi
Behandlingens succes afhænger direkte af rettidig diagnose af sygdommen, som forårsager dannelsen af et protein-polysaccharidkompleks (amyloid) i forskellige organer og leveren. Som praksis viser, er amyloidose vanskelig at antage eller mistænke, selvom det er muligt at identificere og bekræfte den. Faktum er, at i mere end 80% af uopdagede tilfælde er sygdommen klinisk maskeret af leverpatologi. Den mest effektive diagnostiske metode er biopsi.
Leveramyloidose er et sjældnere problem sammenlignet med renal amyloidose. Samtidig ledsages alle tilfælde af leverlæsioner af læsioner i andre organer. Oftest påvirker patologien overvejende strukturelle dele af levertriaden, hvilket bestemmer symptomatologiens minimale og uspecificitet. Det kliniske og morfologiske billede af hepatocellulær defekt og portal hypertension manifesterer sig i diffus og intralobulær patologi.
En leverbiopsi er berettiget, når der er hepatomegali til stede uden tidligere leversymptomer og i fravær af nefrotisk syndrom.
Diffus leverinvolvering ses i omkring 25% af tilfældene, og hos 75% af patienterne er kun portalkanalerne påvirket.
Primær amyloidose påvirker leveren i 90% af tilfældene, mens sekundær amyloidose kun påvirker leveren i 47% af tilfældene.
Isoleret leverpåvirkning er ekstremt sjælden. Nyrer (ca. 93 % af tilfældene), milt (72 %), hjerte (57 %), bugspytkirtel (36 %), binyrer (29 %), tarme og lunger (21 % hver) påvirkes normalt samtidig.
Kvinder får sygdommen næsten dobbelt så ofte som mænd. Den gennemsnitlige forventede levetid for amyloidosepatienter er 52-64 år.
Årsager hepatisk amyloidose
Amyloidose fortsætter med dannelse og akkumulering af et komplekst polysaccharid-proteinkompleks - amyloid - i levervævet. Problemet med forekomsten af den primære læsion er hidtil utilstrækkeligt undersøgt. Hvad angår sekundær patologi, er dens forekomst normalt forbundet med sådanne sygdomme:
- Kroniske infektiøse processer (tuberkulose, syfilis, aktinomykose);
- Purulente inflammatoriske processer (mikrobiel endokarditis, osteomyelitis, bronkiektatisk sygdom osv.);
- Maligne sygdomme (leukæmi, visceral cancer, lymfogranulomatose).
Den reaktive form af amyloidose findes hos patienter med samtidig åreforkalkning, reumatologiske sygdomme (Bechterews sygdom, leddegigt), psoriasis, kroniske inflammatoriske og multisystemprocesser (herunder sarkoidose). De vigtigste risikofaktorer: arvelig prædisposition, cellulære immunitetsforstyrrelser, hyperglobulinæmi.
Patogenese
Der er en række antagelser vedrørende oprindelsen af leveramyloidose. De fleste specialister holder sig til versionen af dysproteinose, sygdommens immunologiske og mutationelle natur samt lokal cellulær genese. Versionen af cellulær genese omfatter ændringer i reaktioner, der virker på celleniveau (dannelse af fibrillære amyloidforløbere af et kompleks af makrofager), selvom amyloid dannes og akkumuleres uden for de cellulære strukturer.
Versionen af dysproteinose er baseret på, at amyloid er et produkt af ukorrekt proteinmetabolisme. Den grundlæggende patogenetiske forbindelse til problemet ligger i dysproteinæmi og hyperfibrinogenæmi, som fører til ophobning af grove dispergerede protein- og paraproteinfraktioner i plasmaet.
Ifølge den immunologiske version forårsages amyloiddannelse af en antigen-antistof-reaktion, hvor vævshindringsprodukter eller fremmede proteiner fungerer som antigener. Amyloid-ophobning findes hovedsageligt i området med antistofdannelse og overdreven tilstedeværelse af antigener.
Den mest plausible version betragter forskere mutationsteorien, som tager højde for en række mutagene faktorer, der kan føre til abnormiteter i proteinsyntesen.
Amyloid er et komplekst hypoprotein, der består af globulære og fibrillære proteiner kombineret med polysaccharider. Amyloid-ophobninger påvirker intima og adventitia i det vaskulære netværk, stroma i parenkymatiske organer, kirtelstrukturen osv. Amyloid-ophobninger forårsager ikke funktionel skade. Små ophobninger forårsager ikke funktionelle forstyrrelser, men ved intens amyloid-tilstedeværelse i leveren øges volumen, organets udseende ændres, og der udvikles funktionsnedsættelse.
Leveramyloidose er karakteriseret ved aflejring af amyloidfibriller i Dysse-rummet, som normalt begynder i den periportale region, selvom den undertiden er centrilobulær og også kan aflejres i leverens vaskulatur. [ 4 ], [ 5 ] I alvorlige tilfælde fører amyloidaflejring til trykatrofi af hepatocytter, hvilket forhindrer passage af galde, hvilket resulterer i kolestase, eller kan blokere sinusoiderne, hvilket resulterer i portal hypertension. [ 6 ], [ 7 ], [ 8 ]
Symptomer hepatisk amyloidose
Det kliniske billede ved leveramyloidose er forskelligartet og afhænger af intensiteten af amyloidakkumulering, dens biokemiske egenskaber, varigheden af den patologiske proces, graden af organskade og forstyrrelser i deres funktionelle tilstand.
I det latente stadie af amyloidose, hvor amyloidophobninger i leveren kun kan detekteres ved mikroskopisk undersøgelse, er de første tegn på sygdommen fraværende. Med yderligere udvikling og stigende funktionelt underskud af organet skrider symptomatologien frem.
Leveren fortykkes gradvist og forstørres. Palpationsmetoden kan ændres, men organets grænser er glatte og smertefrie. I sjældne tilfælde ledsages patologien af smerter i det subkostale område på højre side, dyspepsi, forstørrelse af milten, gulfarvning af hud, slimhinder og senehinde, hæmoragisk syndrom.
De mest karakteristiske symptomer ved leveramyloidose: [ 9 ], [ 10 ]
- Amyloidophobning i leveren forårsager hepatomegali hos 33-92% af patienterne;
- Mild gulsot
- Portal hypertension;
- Moderat til svær kolestase.
Da amyloidose meget sjældent kun påvirker ét organ, er der normalt yderligere symptomer til stede:
- Når nyreskade udvikler nefrotisk syndrom og arteriel hypertension med yderligere nyresvigt, ødem, undertiden nyrevenetrombose, leukocyturi, hæmaturi, hypoproteinæmi, azotæmi og så videre;
- Når hjertet påvirkes, udvikles en tilstand svarende til restriktiv kardiomyopati (rytmeforstyrrelser, kardiomegali, stigende hjertesvigt, svaghed og dyspnø, ødem, sjældnere - væskeophobning i bukhulen og pleurahulen, perikarditis);
- Hvis fordøjelseskanalen er påvirket, kan der forekomme makroglossi, svaghed og øsofageal peristaltik, kvalme og halsbrand, forstoppelse eller diarré osv.;
- Når bugspytkirtlen er påvirket, er symptomerne på kronisk pankreatitis til stede;
- Hvis den muskuloskeletale mekanisme er involveret, udvikles symmetrisk polyarthritis, karpaltunnelsyndrom, myopatier, og hvis nervesystemet påvirkes, findes polyneuropatier, lammelse, ortostatisk lavt blodtryk, øget svedtendens, demens.
Hvis den patologiske reaktion spreder sig til huden, opstår der talrige voksagtige plaques i ansigtet, på halsen og i hudfolderne. Billedet af neurodermatitis, rød pladefeber og sklerodermi er muligt.
Kombinationen af flere amyloidlæsioner og de varierede symptomer gør identifikationen af hepatisk amyloidose meget vanskeligere og kræver en omfattende og komplet diagnose.
Forms
Ifølge WHO-klassificeringen skelnes der mellem fem typer amyloidose:
- AL (primær);
- AA (sekundær);
- ATTR (arvelig og senil systemisk);
- Aβ2M (hos patienter i hæmodialyse);
- AIAPP (hos patienter med insulinuafhængig diabetes mellitus);
- AB (mod Alzheimers sygdom);
- AANF (senil atrieamyloidose).
Der er en lokal amyloidose i leveren, men oftere er det en systemisk læsion, hvor den patologiske proces også involverer nyrerne, hjertet, milten, nervesystemet samt andre organer og væv.
Komplikationer og konsekvenser
Systemisk amyloidose fører gradvist til udvikling af akutte patologiske processer, som igen kan føre til døden. Blandt de mest almindelige og livstruende komplikationer er følgende:
- Hyppige infektiøse (bakterielle, virale) patologier, herunder lungebetændelse, pyelonefritis, glomerulonefritis;
- Kronisk lever- og nyresvigt;
- Kronisk hjertesvigt (kan gå forud for myokardieinfarkt);
- Hæmoragiske slagtilfælde.
Venøs trombose opstår som følge af ophobning og aflejring af proteiner på venevæggene. Lumen i de berørte kar indsnævres, og organsvigt udvikler sig. Over tid, på baggrund af langvarig hyperproteinæmi, kan karret lukke sig helt. Enhver af komplikationerne kan føre til et ugunstigt udfald - døden.
Diagnosticering hepatisk amyloidose
Hvis der er mistanke om leveramyloidose, udføres diagnostiske foranstaltninger efter obligatoriske konsultationer med både gastroenterolog og terapeut, og reumatolog, kardiolog, hudlæge, neurolog, urolog. Det er vigtigt at foretage en omfattende evaluering af anamnese og kliniske manifestationer samt at udføre en omfattende laboratorie- og instrumentel diagnostik.
Testene inkluderer nødvendigvis urin- og blodprøver. Ved hepatisk amyloidose ses ofte en kombination af leukocyturi med proteinuri og cylindruri, og hypoproteinæmi - med hyperlipidæmi, anæmi, hyponatriæmi og hypocalcæmi, reduceret antal blodplader. Paraproteiner detekteres i urin og serumelektroforese.
Instrumentel diagnostik omfatter:
- EKG, Ekko;
- Ultralyd af abdomen;
- Røntgenbilleder af maven, spiserøret;
- Irrigografi, bariumrøntgenstråler;
- Endoskopi.
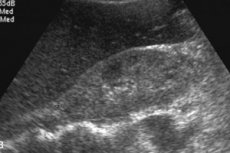
Radiologiske fund af hepatisk amyloidose inkluderer uspecifik hepatomegali, øget ekogenicitet ved ultralyd eller densitet ved computertomografi (CT) og øget T1-signalintensitet ved magnetisk resonansbilleddannelse (MRI). [ 12 ] Scintigrafi med Tc-99m-relaterede indikatorer viser heterogen optagelse, men den er uspecifik. [ 13 ], [ 14 ] GC har vist sig at øge leverstivhed målt ved elastografi; [ 15 ], [ 16 ], [ 17 ], men der er få caserapporter. Magnetisk resonanselastografi (MRE) er i øjeblikket den mest nøjagtige ikke-invasive metode til at detektere og stadiebestemme leverfibrose, [ 18 ], [ 19 ] MRE er nyttig til at detektere progression, respons på behandling og forudsige leverdekompensation hos patienter med leverfibrose. [ 20 ]
Leveramyloidose ved ultralyd er vanskelig at bestemme: en forstørrelse af organet bestemmes, hvor den mest specifikke hepatomegali overstiger 15 cm. Under ultralydskontrol udføres en biopsi, som bliver en afgørende indikator for diagnosen. Ved hjælp af en speciel nål tages en lille mængde levervæv, hvorefter det farves med et specielt farvestof og undersøges under et mikroskop, hvilket giver dig mulighed for direkte at se amyloidaflejringer.
En endelig diagnose stilles først efter påvisning af amyloidfibriller i levervæv og andre organer. Den genetisk bestemte type amyloidose bestemmes ved en omhyggelig genetisk-medicinsk undersøgelse af stamtavlen.
Differential diagnose
Amyloidose bør mistænkes hos alle patienter med en kombination af renal proteinuri, restriktiv kardiomyopati, autonom eller perifer neuropati og hepatomyeli, selv i fravær af monoklonalt paraprotein. Det er meget vigtigt at verificere typen af amyloidose, fordi behandlingen af læsioner af forskellig ætiologi er meget forskellig.
Histologisk diagnose involverer farvning med congorødt efterfulgt af mikroskopisk undersøgelse i polariserende lys. Det tilrådes at biopsiere flere vævsprøver på én gang. Hvis resultatet af farvningen bliver positivt, udføres immunhistokemisk analyse ved hjælp af monoklonale antistoffer mod precursorproteiner for at identificere typen af amyloid.
DNA-analyse udføres for at skelne mellem primær amyloidose og forskellige variationer af genetisk bestemt amyloidose. Amyloidfibriller kan isoleres fra biopsiprøver og sekvestreres i individuelle aminosyrer.
Yderligere undersøgelser for at bestemme plasmacelledyskrasi:
- Elektroforese af serumproteiner i blod og urin;
- Immunoassay for frie lette kæder;
- Immunfiksering (immunoblotting) af serumproteiner;
- Knoglemarvsaspiration og trepanobiopsi.
Diagnose af leveramyloidose er en langvarig og arbejdskrævende proces, som kræver øget opmærksomhed fra specialister og kvalitetsudstyr fra klinikker og laboratorier.
Hvem skal kontakte?
Behandling hepatisk amyloidose
Behandlingsforanstaltningerne har til formål at reducere koncentrationen af præeksisterende amyloidproteiner i blodet (eliminere årsagen til amyloidose) og understøtte tilstrækkelig leverfunktion.
Sekundær amyloidose kræver blokering af den inflammatoriske proces (ved kroniske infektiøse og autoimmune patologier). Ved autoimmune sygdomme anbefales brug af cytostatika. For at eliminere kroniske infektiøse processer fjernes det inflammerede område ofte kirurgisk. Denne tilgang kan ofte stoppe yderligere progression af amyloidose og forbedre leverfunktionen.
Primær amyloidose kræver brug af kemopræventive lægemidler og undertiden knoglemarvstransplantation.
Nuværende retningslinjer anbefaler kombinationen af cyclophosphamid, bortezomib, dexamethason (CyBorD) og daratumumab som førstelinjebehandling hos patienter, der nydiagnosticeres med AL.
Bortezomib er en proteasomhæmmer. Proteasomer er involveret i at reducere proteotoksicitet og regulere proteiner, der kontrollerer cellulær progression og apoptose. Plasmaceller, der genererer amyloid, er særligt følsomme over for proteasomhæmning, fordi de er afhængige af proteasomet til at reducere de toksiske virkninger af lette kæder og forhindre apoptose.
Daratumumumab er et monoklonalt antistof (mAb), der binder til CD38, et transmembrant glykoprotein udtrykt på overfladen af plasmaceller, hvilket inducerer apoptose. Det er det eneste lægemiddel, der er specifikt godkendt til behandling af AL-amyloidose, når det anvendes sammen med CyBorD. Effekten af CyBorD-daratumumumab er meget høj, hvor 78 % af patienterne opnår et signifikant hæmatologisk respons (defineret som et komplet respons eller et meget godt delvist respons). Median overlevelse i den lille gruppe af patienter, der fik CyBorD (n = 15), var 655 dage sammenlignet med 178 dage for patienter, der fik anden melphalan-dexamethason-baseret behandling (n = 10).4
Disse behandlinger har imidlertid adskillige bivirkninger, herunder kardiotoksicitet, hvilket fører til behov for dosisreduktion eller afbrydelse af behandlingen samt brugen af andre mindre effektive, men mere tålelige terapeutiske strategier.
Isatuximab, et monoklonalt antistof mod CD38 svarende til daratumumab, undersøges til behandling af plasmacelledyskrasi, der ligger til grund for AL.
Tre monoklonale antistoffer, birtamimab, CAEL-101 og AT-03, undersøges i øjeblikket til fjernelse af amyloidfibriller fra syge organer. Resultaterne af disse undersøgelser vil kunne give direkte bevis for hypotesen om, at fjernelse af letkædedepositionsfibriller fra organer medfører en forbedring af organfunktionen. [ 21 ]
For at understøtte leverfunktionen ordineres lægemidler baseret på urso-deoxycholsyre (f.eks. Ursosan). Urso-deoxycholsyre hjælper med at stabilisere cellemembraner, reducerer den negative virkning af giftige fedtsyrer i galdestasis fremkaldt af amyloidaflejringer og hjælper med at genoprette normal galdeudstrømning.
Derudover symptomatisk behandling og støtte til funktionen af andre vitale strukturer såsom nervesystem, hjerte, nyrer osv. Støttende behandling til patienter med hepatisk amyloidose omfatter forskellige kliniske aspekter, herunder behandling af hjertesvigt, arytmier, ledningsforstyrrelser, tromboembolisme og samtidig tilstedeværelse af aortastenose.
Andre behandlinger afhænger af typen af amyloidose og hvilke dele af kroppen der er berørt. Behandlinger kan omfatte: [ 22 ]
- Medicin, der lindrer symptomer, såsom smertestillende midler, medicin mod kvalme eller medicin, der reducerer hævelse (diuretika);
- Medicin til at reducere amyloid;
- Nyredialyse;
- Levertransplantation.
Leveren producerer 95% af TTR (transthyretin, et protein involveret i thyroxin (T4) transport og retinol-bindende protein. Transthyretin syntetiseres hovedsageligt i leveren og er rig på beta-strenge, der har tendens til at aggregere til uopløselige amyloidfibriller) målt i serum. Derfor er levertransplantation historisk set (siden 1990) blevet foreslået som førstelinjebehandling for at eliminere den primære kilde til amyloidogen TTR hos patienter med den familiære form (ATTRv), hvorimod det ikke er indiceret i ATTR-wt-formen. Levertransplantation af unge patienter i de tidlige stadier af sygdommen er forbundet med en høj 20-års overlevelsesrate. Levertransplantation synes at være mere effektiv i nogle mutationer og mindre effektiv i andre, såsom V122I (associeret med kardiomyopati). Kombineret lever- og hjertetransplantation er også mulig hos unge ATTRv-patienter med kardiomyopati, og litteraturdata om en lille gruppe patienter tyder på, at denne kombination har en bedre prognose end hjertetransplantation alene.
Patienter med hepatisk amyloidose er kontraindiceret til at tage hjerteglykosider og calciumantagonister såsom Diltiazem eller Verapamil, som kan ophobes i amyloid. ACE-hæmmere og beta-adrenoblokkere anvendes med forsigtighed.
Ved ortostatisk hypotension ordineres mineralokortikoider eller glukokortikoider, idet der tages højde for, at de kan forårsage dekompensation af hjertesvigt. Det alfa-adrenomimetiske lægemiddel midodrin (Gutron) anvendes også med forsigtighed.
Antikonvulsiva og antidepressiva er passende ved neuropatier.
I nogle tilfælde af leveramyloidose er lægerne nødt til at overveje organtransplantation.
Forebyggelse
På grund af manglende information om patogenesen af leveramyloidose kan specialister ikke udvikle en specifik forebyggelse af sygdommen. Derfor er den primære indsats reduceret til rettidig opdagelse og behandling af eventuelle kroniske patologier, der kan provokere udviklingen af lidelsen. Hvis der er tilfælde af amyloidose af en hvilken som helst lokalisering i familien, anbefales det systematisk at besøge læger for at få foretaget undersøgelser på apoteket.
Generelt reduceres forebyggende foranstaltninger til rettidig eliminering af infektionssygdomme, især dem, der har tendens til at udvikle sig til en kronisk proces. Det handler om at forhindre udviklingen af tuberkulose, lungeinfektioner osv. Det er vigtigt med rettidig opdagelse og tilstrækkelig behandling af streptokokinfektioner, som kan blive årsag til kroniske former for autoimmune inflammatoriske processer. Vi taler om scarlatina, streptokokbetændelse i mandlen osv.
Hvis patienten allerede har en autoimmun sygdom, bør han systematisk konsultere en læge, observere patologiens aktivitet, anvende de nødvendige lægemidler som ordineret af lægen, justere doseringen i henhold til indikationerne.
Vejrudsigt
Prognosen for patienter med hepatisk amyloidose er ugunstig. Sygdommen forværres langsomt, men kontinuerligt, hvilket i sidste ende forårsager dysfunktion af de berørte organer og dødelig udgang - især på grund af organsvigt.
Patienter med systemisk patologi dør hovedsageligt som følge af udviklingen af kronisk nyresvigt, selvom hæmodialyse eller kontinuerlig ambulant peritonealdialyse i nogle tilfælde forbedrer prognosen for sådanne patienter. Overlevelsesraten for patienter i hæmodialyse, uanset type, kan sammenlignes med overlevelsesraten for personer med andre systemiske patologier og diabetes mellitus.
Hovedårsagen til død under hæmodialyse er udviklingen af komplikationer fra det kardiovaskulære system.
Levertransplantation har længe været betragtet som en af de vigtigste behandlingsmetoder for sygdommen, og de mest optimistiske overlevelsesrater observeres hos patienter, hvis alder ikke overstiger 50 år (forudsat at den patologiske proces er kortvarig, og kropsmasseindekset er normalt). Patienter med leveramyloidose kombineret med perifer neuropati har en noget dårligere prognose.

