Nye publikationer
Afklaring af de cellulære mekanismer i parodontitis med en forbedret dyremodel
Sidst revideret: 02.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Forskere fra Tokyo Medical and Dental University (TMDU) har udviklet en teknik, der muliggør detaljeret analyse af udviklingen af parodontitis over tid.
Paradentose, kendt som parodontitis, er den hyppigste årsag til tandtab og rammer næsten hver femte voksen på verdensplan. I de fleste tilfælde skyldes tilstanden en inflammatorisk reaktion på en bakteriel infektion i vævet omkring tænderne.
Efterhånden som tilstanden forværres, begynder tandkødet at trække sig tilbage, hvilket blotlægger tændernes og knoglernes rødder. Det er værd at bemærke, at forekomsten af parodontitis stiger med alderen, og da verdens befolkning lever længere, er det vigtigt at have en solid forståelse af dens underliggende årsager og progression.
I et studie offentliggjort i tidsskriftet Nature Communications fandt forskere fra TMDU en måde at opnå dette mål på ved at forbedre en udbredt dyremodel til studier af parodontitis.
Det er vanskeligt at studere parodontitis direkte hos mennesker. Som følge heraf vender forskere sig ofte mod dyremodeller til prækliniske studier. For eksempel har "ligaturinduceret parodontitis-musemodel" gjort det muligt for forskere at studere de cellulære mekanismer, der ligger til grund for tilstanden, siden dens introduktion i 2012.
Enkelt sagt fremkalder denne model kunstigt parodontose ved at placere silketråde på kindtænderne hos mus, hvilket forårsager ophobning af plak. Selvom denne metode er bekvem og effektiv, indfanger den ikke det fulde billede af parodontitis.
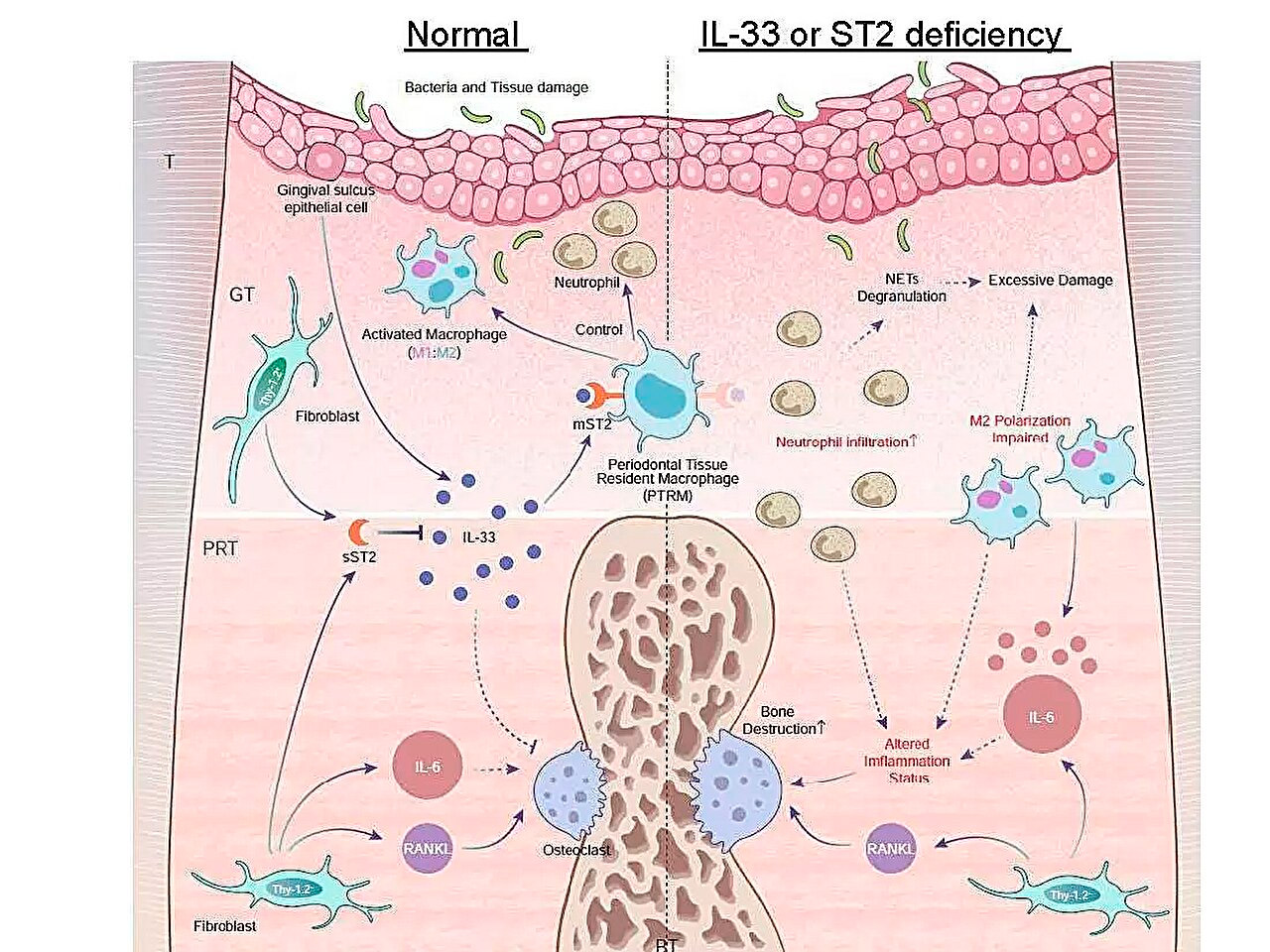
Skematisk illustration af inflammatoriske genekspressionsprofiler under parodontitis og IL-33/ST2-aksens rolle i bekæmpelsen af akut inflammation. Kilde: Tokyo Medical and Dental University.
"Selvom parodontalt væv består af gingiva, parodontalligament, alveolær knogle og cement, udføres analysen typisk udelukkende på gingivaprøver på grund af tekniske og kvantitative begrænsninger," bemærker hovedforfatter af studiet, Anhao Liu. "Denne prøveudtagningsstrategi begrænser de konklusioner, der kan drages fra disse undersøgelser, så der er behov for metoder, der muliggør samtidig analyse af alle vævskomponenter."
For at imødegå denne begrænsning udviklede forskerholdet en modificeret ligaturinduceret parodontitismodel. I stedet for den klassiske enkeltligatur brugte de en tredobbelt ligatur på den øverste venstre molar hos hanmus. Denne strategi udvidede området med knogletab uden at ødelægge knoglen omkring den anden molar væsentligt, hvilket øgede antallet af forskellige typer parodontalt væv.
"Vi isolerede tre hovedvævstyper og vurderede RNA-udbyttet mellem de to modeller. Resultaterne viste, at den triple-ligerede model effektivt øgede udbyttet, opnåede fire gange mængden af normalt periradikulært væv og understøttede højopløsningsanalyse af forskellige vævstyper," forklarer seniorforfatter Dr. Mikihito Hayashi.
Efter at have bekræftet effektiviteten af deres modificerede model, satte forskerne sig for at undersøge virkningerne af parodontitis på genekspression på tværs af forskellige vævstyper over tid, med fokus på gener forbundet med inflammation og osteoklastdifferentiering.
Et af deres vigtigste fund var, at ekspressionen af Il1rl1-genet var signifikant højere i det periradikulære væv fem dage efter ligering. Dette gen koder for ST2-proteinet i receptor- og decoy-isoformer, som binder til et cytokin kaldet IL-33, som er involveret i inflammatoriske og immunregulerende processer.
For at få yderligere indsigt i dette gens rolle inducerede teamet parodontitis i genetisk modificerede mus, der manglede enten Il1rl1- eller Il33-generne. Disse mus udviste accelereret inflammatorisk knogledestruktion, hvilket fremhæver den beskyttende rolle af IL-33/ST2-signalvejen. Yderligere analyse af celler, der indeholder ST2-proteinet i dets receptorform, mST2, afslørede, at de fleste af dem stammede fra makrofager.
"Makrofager klassificeres generelt i to hovedtyper, proinflammatoriske og antiinflammatoriske, afhængigt af deres aktivering. Vi fandt, at mST2-udtrykkende celler var unikke, idet de samtidig udtrykte nogle markører for begge typer makrofager," kommenterede seniorforfatter Dr. Takanori Iwata. "Disse celler var til stede i det periradikulære væv, før inflammationen begyndte, så vi kaldte dem 'parodontale vævsresidente makrofager'."
Samlet set demonstrerer resultaterne af dette studie, hvilken effekt en modificeret dyremodel har på at studere parodontitis i en mere detaljeret skala, ned til det biomolekylære niveau.
"Vi foreslår muligheden for en ny IL-33/ST2 molekylær signalvej, der regulerer inflammation og knogledestruktion i parodontal sygdom, sammen med specifikke makrofager i det periradikulære væv, der er dybt involveret i parodontal sygdom. Dette vil forhåbentlig føre til udvikling af nye behandlingsstrategier og forebyggelsesmetoder," konkluderer seniorforfatter Dr. Tomoki Nakashima.
