Nye publikationer
FDA-godkendt TIVDAK®: Målrettet mod vævsfaktor i livmoderhalskræft
Sidst revideret: 02.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Den 29. april 2024 gav den amerikanske fødevare- og lægemiddelstyrelse (FDA) fuld godkendelse til Seagen Inc.'s TIVDAK® (tisotumab vedotin), et lægemiddel målrettet mod vævsfaktor (TF), til behandling af patienter med tilbagevendende eller metastatisk livmoderhalskræft, der er progredieret under eller efter kemoterapi. Dette repræsenterer et betydeligt gennembrud inden for behandling af livmoderhalskræft og fremhæver potentialet for antistoflægemiddelkonjugater (ADC'er) inden for onkologi.
Virkningsmekanisme for TIVDAK
Tivdak er et ADC, der målretter TF ved at kombinere Genmabs monoklonale anti-TF-antistof tisotumab med Seagens ADC-teknologi, der er designet til at målrette TF-antigener på kræftceller og levere den cytotoksiske komponent MMAE direkte til kræftcellerne.
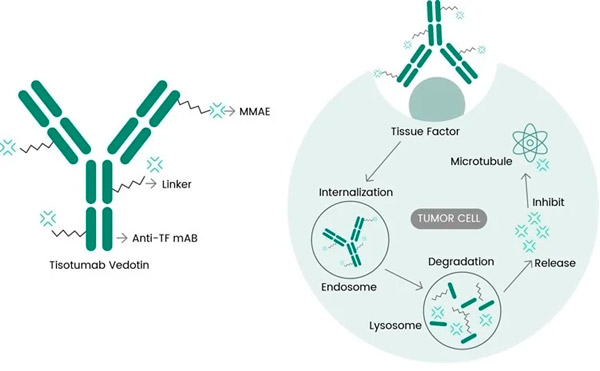
Molekylær virkningsmekanisme for tisotumab vedotin ( https://doi.org/10.3390/ijms23073559 )
TF: Det perfekte mål for ADC-udvikling
TF er kendt for at være involveret i tumorsignalering og angiogenese og er overudtrykt hos langt de fleste patienter med livmoderhalskræft og mange andre solide tumorer. Dets evne til hurtigt at blive internaliseret ved antistofbinding og dets minimale indvirkning på normal blodkoagulation forbedrer yderligere dets egnethed til målrettet kræftbehandling.
