Nye publikationer
Nyt studie forklarer svækket immunrespons hos ældre
Sidst revideret: 02.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Et fuldt fungerende immunsystem er afgørende for at opretholde kroppens sundhed, og makrofager spiller en afgørende rolle i at opretholde stærke immunresponser mod infektioner.
En makrofag er en type hvide blodlegemer, der ødelægger mikroorganismer, fjerner døde celler og stimulerer andre immuncellers aktivitet. Disse celler spiller en nøglerolle i at initiere, opretholde og løse inflammation, men deres funktionalitet falder med alderen, hvilket fører til et fald i immunforsvaret. Dette fører til øget modtagelighed for infektioner og autoimmune sygdomme hos den ældre befolkning.
En undersøgelse offentliggjort i tidsskriftet Cell Reports er den første til at afsløre, at defekter i makrofagfunktionen er forårsaget af MYC- og USF1-transkriptionsprogrammerne.
Forskning ledet af Charlotte Moss, Dr. Heather Wilson og professor Endre Kiss-Toth har identificeret en mulig synder for dette fald: to kritiske molekyler inde i makrofager, MYC og USF1, som begynder at fungere forkert, når vi ældes.
Makrofager, ofte omtalt som kroppens "skraldevogne", er ansvarlige for at opsluge og eliminere fremmede partikler, herunder affald og patogener. En undersøgelse viste, at makrofager isoleret fra ældre voksne var signifikant mindre effektive end makrofager fra yngre voksne. Disse aldrende makrofager udviste nedsat fagocytose (processen med at opsluge fremmede partikler) og forringet kemotaksi (evnen til at migrere mod trusler).
Forskerne bekræftede denne sammenhæng ved kunstigt at reducere aktiviteten af MYC og USF1 i unge makrofager. Denne manipulation resulterede i et funktionelt fald, der mindede om makrofager fra ældre voksne. Dette fund tyder stærkt på, at MYC og USF1 spiller en vigtig rolle i at opretholde optimal makrofagfunktion.
Undersøgelsen går ud over blot at identificere synderne. Den undersøger, hvordan nedsat aktivitet af MYC og USF1 kan påvirke makrofager. Forskerne spekulerer i, at disse ændringer kan forstyrre gener, der er ansvarlige for cellens indre cytoskelet, et netværk af tråde, der giver struktur og bevægelse.
Denne forstyrrelse kan påvirke makrofagens evne til at bevæge sig og opsluge fremmede partikler. Derudover kan ændret MYC- og USF1-aktivitet påvirke, hvordan makrofager interagerer med deres omgivelser, hvilket yderligere forringer deres evne til at bekæmpe infektion.
Denne undersøgelse repræsenterer et betydeligt gennembrud i forståelsen af mekanismerne bag aldersrelateret immunforsvarsnedbrydning.
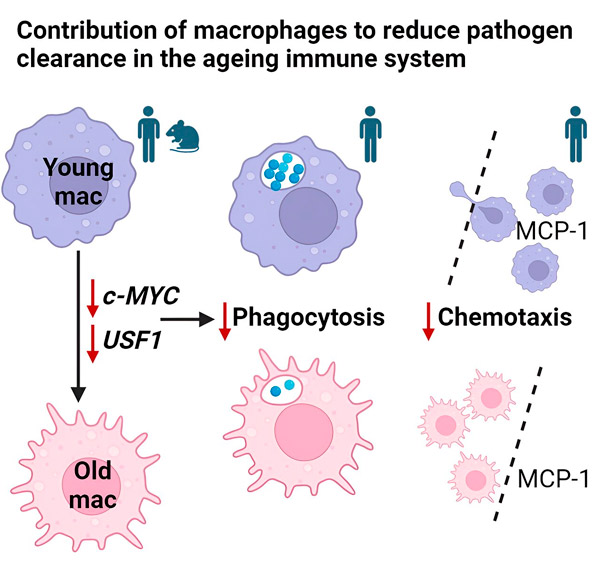
Grafisk figur. Kilde: Cell Reports (2024). DOI: 10.1016/j.celrep.2024.114073
Ved at identificere MYC og USF1 som potentielle syndere baner studiet vejen for udviklingen af nye terapeutiske strategier. Ved at målrette disse molekyler eller deres genprodukter kan forskere muligvis forbedre makrofagfunktionen hos ældre voksne, hvilket kan føre til et stærkere immunrespons og forbedret modstandsdygtighed over for infektioner.
Det er vigtigt at bemærke, at studiet omfattede raske frivillige og ikke personer med præeksisterende aldersrelaterede sygdomme. Derudover blev studierne udført i et kontrolleret laboratoriemiljø. Yderligere undersøgelser er nødvendige for at bekræfte disse resultater i en større population og for at undersøge muligheden for at omsætte disse resultater til effektive behandlinger.
Identifikationen af MYC og USF1 som potentielle mål for intervention repræsenterer et betydeligt skridt fremad. Denne undersøgelse åbner op for udviklingen af fremtidige strategier til at styrke immunforsvaret hos ældre voksne og i sidste ende fremme en sundere aldring.
"At forstå, hvorfor immunsystemet holder op med at bekæmpe infektioner effektivt i alderdommen, er nøglen til at udvikle behandlinger, der kan vende denne proces. Vores arbejde afslører for første gang de molekylære detaljer ved aldring i menneskelige fagocytter, og vi mener, at denne nye forståelse nu giver os mulighed for at teste effektiviteten af forskellige interventioner, herunder kost, livsstil og endda potentielle lægemidler, der sigter mod at vende immunsystemets aldring," siger Endre Kiss-Toth.
