Nye publikationer
Nyt studie afslører mitokondrieproteiners nøglerolle i hjertefornyelse
Sidst revideret: 02.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Mitokondrier spiller en afgørende rolle i at levere den energi, der er nødvendig for korrekt cellefunktion. I mitokondrier produceres energi af respirationskæden, som består af fem komplekser, betegnet CI-CV. Disse komplekser kan samles i superkomplekser, men der vides kun lidt om denne process rolle og dens kontrol.
Det nye studie undersøger mekanismerne bag superkompleks-samling og afslører en betydelig indvirkning af mitokondrielle samlingsfaktorer på regenerering af hjertevæv. Studiet blev ledet i fællesskab af Dr. José Antonio Enríquez fra National Center for Cardiovascular Research (CNIC) og Dr. Nadia Mercader fra Berns Universitet i Schweiz, som er gæsteforsker ved CNIC.
Et studie offentliggjort i tidsskriftet Developmental Cell viser, at proteinfamiliemedlemmet Cox7a spiller en fundamental rolle i sammensætningen af CIV-dimerer, og at denne sammensætning er afgørende for mitokondriernes korrekte funktion og dermed for cellulær energiproduktion.
Cox7a-proteinfamilien omfatter tre medlemmer: Cox7a1, Cox7a2 og Cox7a2l (også kaldet SCAF1). Tidligere undersøgelser foretaget af begge grupper har vist, at når CIV indeholder SCAF1, associerer det stærkt med CIII og danner et respiratorisk superkompleks kendt som respirasomet. I disse tidligere undersøgelser fremsatte forfatterne hypotesen om, at inkludering af Cox7a2 ville resultere i et CIV, der ikke er i stand til at associere, mens CIV-molekyler, der indeholder Cox7a1, ville associere og danne CIV-homodimerer. Det nye studie demonstrerer eksperimentelt en rolle for Cox7a1 i dannelsen af disse CIV-homodimerer.
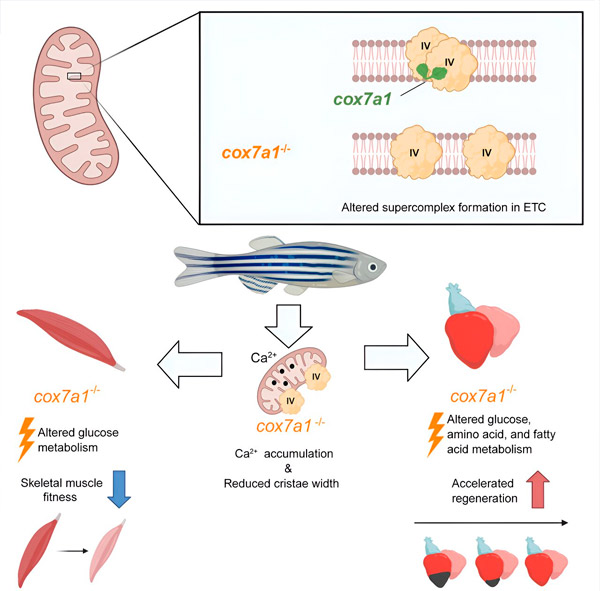
Udviklingscelle (2024). DOI: 10.1016/j.devcel.2024.04.012
Ved at arbejde med en zebrafiskmodel fandt forskerne, at fraværet af Cox7a1 forhindrede dannelsen af CIV-dimerer, og tabet af disse dimerer påvirkede de berørte fisks vægt og svømmeevne.
"Cox7a1 udtrykkes primært i tværstribede muskelceller, og det var skeletmuskelvæv, der led mest under manglen på Cox7a1-funktion. Den anden vigtige type tværstribede muskler er hjertemusklen eller myokardiet," forklarede Dr. Enriquez.
Men mens tabet af Cox7a1 i skeletmuskulatur var skadeligt, forbedrede dets fravær i hjertemuskulaturen den kardiale regenerative respons på skade.
"Dette resultat viser, at disse proteiner spiller en nøglerolle i at aktivere hjertets evne til at reparere sig selv efter en skade," forklarede Carolina Garcia-Pojatos, førsteforfatter af studiet.
For yderligere at undersøge funktionen af Cox7a1 udførte CNIC-forskerne Enrique Calvo og Jesús Vásquez en proteomisk undersøgelse af skeletmuskulatur og myokardium hos zebrafisk, der mangler Cox7a1. Denne analyse blev suppleret af en metabolomisk undersøgelse udført af kolleger ved Berns Universitet. Denne kombinerede analyse afslørede signifikante forskelle fra umodificerede fisk med intakt Cox7a1-ekspression.
"Disse resultater tyder på, at molekyler involveret i sammensætningen af mitokondrielle superkomplekser kan have betydelige virkninger på metabolisk kontrol, hvilket muligvis åbner vejen for nye behandlinger af hjertesygdomme og andre metaboliske lidelser," sagde Dr. Mercader.
Ifølge forskerholdet repræsenterer denne opdagelse "et betydeligt skridt fremad i forståelsen af de cellulære mekanismer, der er involveret i hjerteregenerering, og kan pege vejen for udviklingen af terapier, der sigter mod at stimulere hjerteregenerering."
Forfatterne konkluderer, at mitokondrielle samlingsfaktorer kan have betydelig indflydelse på metabolisk kontrol.
