Nye publikationer
Kræftceller aktiverer øjeblikkeligt energiproduktion, når DNA komprimeres og beskadiges
Sidst revideret: 03.08.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
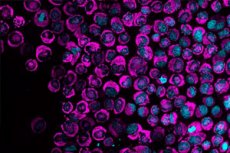
Kræftceller aktiverer øjeblikkeligt en energirig reaktion på fysisk kompression, ifølge et studie offentliggjort i tidsskriftet Nature Communications. Dette energiudbrud er den første dokumenterede manifestation af en beskyttelsesmekanisme, der hjælper celler med at reparere beskadiget DNA og overleve de trange forhold i menneskekroppen.
Disse resultater hjælper med at forklare, hvordan kræftceller overlever i komplekse mekaniske miljøer, såsom at kravle gennem tumormikromiljøer, trænge ind i porøse blodkar eller overvinde stød i blodbanen. Opdagelsen af mekanismen kan føre til nye strategier til at "forankre" kræftceller, før de spreder sig.
Forskere ved Centre for Genomic Regulation (CRG) i Barcelona gjorde opdagelsen ved hjælp af et specialiseret mikroskop, der er i stand til at presse levende celler ned til blot tre mikrometer i bredden – omkring tredive gange mindre end diameteren af et menneskehår. De observerede, at mitokondrierne i HeLa-celler inden for få sekunder efter at være blevet komprimeret, skyndte sig op til overfladen af kernen og begyndte at pumpe ekstra ATP ind, cellernes molekylære energikilde.
"Dette tvinger os til at gentænke mitokondriernes rolle i menneskekroppen. De er ikke bare statiske batterier, der driver celler, men snarere kloge 'redningsmænd', der kan tilkaldes i en nødsituation, når en celle bogstaveligt talt er presset til sine grænser," siger Dr. Sarah Sdelchy, medforfatter til undersøgelsen.
Mitokondrierne dannede en så tæt "glød" omkring cellekernen, at kernen blev presset indad. Dette fænomen blev observeret i 84 procent af de komprimerede HeLa-kræftceller, sammenlignet med næsten nul i de flydende, ukomprimerede celler. Forskerne kaldte disse strukturer NAM, for nucleus-associated mitochondria (kerneassocierede mitokondrier).
For at finde ud af, hvad NAM'er gjorde, brugte forskerne en fluorescerende sensor, der lyser op, når ATP kommer ind i cellekernen. Signalet steg med omkring 60 % blot tre sekunder efter, at cellerne blev presset sammen.
"Dette er et tydeligt tegn på, at cellerne tilpasser sig stresset og omkonfigurerer deres stofskifte," forklarer Dr. Fabio Pezzano, første medforfatter af studiet.
Yderligere eksperimenter viste, hvorfor dette energiboost er vigtigt. Mekanisk kompression stresser DNA, hvilket ødelægger strengene og sammenfiltrer genomet. Celler har brug for ATP-afhængige reparationskomplekser for at svække DNA-strukturen og komme til skaden. Komprimerede celler, der modtog ekstra ATP, reparerede deres DNA inden for få timer, hvorimod celler uden den ekstra ATP holdt op med at dele sig normalt.
For at bekræfte betydningen af denne mekanisme i sygdommen undersøgte forskerne også brysttumorbiopsier fra 17 patienter. NAM-haloer blev observeret i 5,4% af kernerne ved tumorens invasive kant, sammenlignet med 1,8% i den tætte kerne - en tredobbelt forskel.
"Det faktum, at vi fandt denne signatur i patientvæv, bekræftede dens betydning uden for laboratoriet," forklarer Dr. Ritobrata (Rito) Ghose, studiets første medforfatter.
Forskerne var også i stand til at studere de cellulære mekanismer, der muliggør den mitokondrielle "oversvømmelse". Actinfilamenter - de samme proteintråde, der tillader muskler at trække sig sammen - danner en ring omkring cellekernen, og det endoplasmatiske reticulum trækker den netlignende "fælde" sammen. Denne kombinerede ordning, viste undersøgelsen, holder fysisk NAM på plads og danner en "halo". Da forskerne behandlede cellerne med latrunculin A, et lægemiddel, der forstyrrer actin, forsvandt NAM-dannelsen, og ATP-niveauerne faldt drastisk.
Hvis metastatiske celler er afhængige af NAM-associerede ATP-udbrud, kan lægemidler, der forstyrrer stilladset, gøre tumorer mindre invasive uden at forgifte mitokondrierne selv eller påvirke sundt væv.
"Mekaniske stressreaktioner er en dårligt forstået sårbarhed hos kræftceller, der kan åbne op for nye terapeutiske tilgange," sagde Dr. Verena Ruprecht, medforfatter til undersøgelsen.
Selvom studiet fokuserede på kræftceller, påpeger forfatterne, at dette sandsynligvis er et universelt fænomen i biologien. Immunceller, der passerer gennem lymfeknuder, neuroners vækstprocesser og embryonale celler under morfogenese, oplever alle lignende fysisk stress.
"Hvor celler er under pres, beskytter energibølgen til cellekernen sandsynligvis genomets integritet," konkluderer Dr. Sdelchi. "Dette er et helt nyt niveau af regulering inden for cellebiologi, der repræsenterer et fundamentalt skift i vores forståelse af, hvordan celler overlever fysisk stress."
