Undersøgelse af mekanismen for lægemiddelinduceret hududslæt
Sidst revideret: 14.06.2024

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
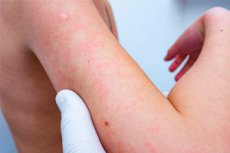
Selvom medicin ofte hjælper patienter med at komme sig eller forbedre deres tilstand, lider millioner af mennesker over hele verden af uforudsigelige toksiske reaktioner på medicin hvert år. Især lægemiddeludslæt, som viser sig med symptomer som rødme, blærer og kløe i huden, er ret almindelige.
Alvorlige lægemiddeludslæt kan blive livstruende og have langvarige virkninger. Derfor er forståelsen af, hvordan og hvorfor lægemiddeludslæt opstår, et vigtigt forskningsområde inden for lægevidenskaben.
Til dette formål har tidligere undersøgelser identificeret specifikke varianter i visse gener som potentielle årsagsstoffer til lægemiddeludbrud. Forskere mener, at gener, der koder for humant leukocytantigen (HLA), et protein udtrykt på overfladen af hvide blodlegemer, som spiller en vigtig rolle i immunsystemet, er involveret i lægemiddeludslæt. De nuværende teorier kan dog ikke forklare, hvorfor HLA-associerede lægemiddeludbrud typisk forekommer på huden snarere end i flere organer i hele kroppen.
For at afhjælpe denne videnskløft gennemførte et forskerhold, herunder fakultetsmedlemmer Shigeki Aoki, Kousei Ito og Akira Kazaoka fra Chiba Universitets Graduate School of Medical and Pharmaceutical Sciences, en dybdegående undersøgelse af forholdet mellem HLA og lægemiddeludbrud. Deres resultater blev offentliggjort i PNAS Nexus.
Forskerne udførte først en række eksperimenter på muse-keratinocytter, som er den primære type celler, der findes i huden. Disse keratinocytter er blevet modificeret til at udtrykke en specifik variant af HLA-genet kaldet HLA-B57:01, som specifikt binder til det antivirale lægemiddel abacavir. De bekræftede derefter disse resultater i gensplejsede mus, der udtrykker HLA-B57:01, som blev udsat for abacavir.
Forskere fandt ud af, at keratinocytter, der udtrykker HLA-B*57:01 og eksponeret for abacavir, udviste endoplasmatisk retikulum (ER) stressreaktioner, såsom øjeblikkelig frigivelse af calcium til cytosolen og øget ekspression af varmechokprotein 70 (HSP70). De observerede også øget cytokinproduktion og migration af immunceller. Eksponering for abacavir forårsagede fejlfoldning af HLA i skadestuen, hvilket førte til akut stress.
Yderligere har forskere fundet ud af, at ER-stress kan reduceres ved at bruge 4-phenylbutyrat (4-PB). Ved at eliminere denne stress var de i stand til at undertrykke begyndelsen af alvorlige lægemiddeludslætssymptomer. Denne nye viden kan danne grundlag for innovative behandlingsmuligheder for lægemiddeludslæt.
Men hvordan står denne nye information i kontrast til, hvad der allerede var kendt om HLA?
"HLA-molekyler er en integreret komponent af vores immunsystem, som typisk præsenterer fremmede antigener for hvide blodlegemer, som vurderer disse antigener som sig selv eller ikke-selv. I denne etablerede rolle spiller HLA'er normalt en mindre rolle," forklarer Dr. Aoki.
"Vores undersøgelse fremhæver imidlertid en ny funktion af HLA-molekylet i hudceller. Vi fandt ud af, at en specifik HLA-genotype i keratinocytter kan genkende visse lægemidler som fremmede, hvilket forårsager en endoplasmatisk retikulum-stressrespons."
Samlet afslører resultaterne af denne undersøgelse en ny rolle for HLA-proteiner i at detektere og reagere på potentielle trusler i hudceller. Deres funktioner kan således strække sig langt ud over den simple præsentation af antigener til immunsystemet. Da en persons HLA-variant kan bestemmes gennem genetisk testning, kan denne forskning desuden hjælpe med at udvikle forebyggende foranstaltninger og diagnostiske metoder mod alvorlige bivirkninger af lægemidlet.
Ifølge Dr. Aoki er dette i tråd med aktuelle retninger og tendenser inden for lægevidenskaben. "Om 10 år forventer vi at gå ind i 'hele genomets' æra, hvor personlig medicin baseret på individuelle genomer vil blive standardpraksis," kommenterer han.
"Baseret på resultaterne af denne undersøgelse mener vi, at en omfattende forståelse af mekanismen bag HLA-afhængige bivirkninger vil muliggøre sikker sundhedspleje, samtidig med at patienter kan undgå unødvendig lidelse på grund af bivirkninger."
Samlet set kan fremtidig forskning på dette område minimere forekomsten af lægemiddeludslæt og redde folk fra potentielt fatale bivirkninger.
