Nye publikationer
Neuroprotese til mave-tarmkanalen: genopretter peristaltikken og aktiverer "mæthedshormoner"
Sidst revideret: 18.08.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
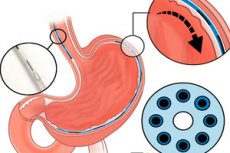
Gastrointestinale (spiserør og mave) motilitetsforstyrrelser - achalasi, gastroparese, dysfagi osv. - rammer mere end 20% af befolkningen og forårsager betydelig sygelighed og omkostninger. Standardtilgange - medicin, adfærdsinterventioner og kirurgi - har ofte begrænset effektivitet og genopretter ikke koordineret peristaltik.
- Hvorfor eksisterende apparater ikke løser problemet. Elektrisk stimulering af mave-tarmkanalen er blevet undersøgt siden 1960'erne, men klinisk godkendte implantater (f.eks. Enterra til gastroparese, VBLOC vagusstimulatorer til fedme, InterStim sakral stimulering til fækal inkontinens) fungerer primært i et åbent kredsløb og har ofte inkonsistente effekter på mavetømning. Årsagen er, at en eller flere strømkilder med konstante parametre ikke reproducerer den spatiotemporale kompleksitet af naturlig peristaltik.
- Fysiologi, der skal "imiteres". Peristaltik er et lukket kredsløb: sensoriske signaler (stræk, temperatur, kemiske stimuli) → refleksresponser i myenteric plexus og glat muskulatur. Ud over fødetransport påvirker motilitet afferente tarm-hjernesignaler og mæthedshormoner (GLP-1, insulin, ghrelin), hvilket danner appetit og en følelse af mæthed. Ved dysmotilitet er disse kredsløb forstyrret.
- Teknologisk hul. For at reproducere de "korrekte" bølger er multikanalstimulation nødvendig direkte nær myenterisk plexus og muskellaget. Adgang dertil kræver dog normalt invasiv kirurgi; avancerede endoskopiske teknikker (f.eks. NOTES) er komplekse og ikke udbredte. Minimalt invasive instrumenter er nødvendige, der muliggør præcis placering af elektroder i submucosa og fungerer i et lukket "registrerings- → stimulerings"-loop.
- Hvad det nye arbejde tilbyder. Forfatterne beskriver en endoskopisk installeret, flerkanals neuroprotese med elektrisk og kemisk stimulering, der er i stand til at udløse koordinerede peristaltiske bølger ved et signal om passage af en bolus, og derved ikke blot genoprette motiliteten, men også modulere det metaboliske respons (bringe det tættere på en "fodret" tilstand). Dette lukker vigtige huller: adgang til det ønskede lag, spatiotemporal koordination og arbejde i et lukket kredsløb.
Kort sagt: der er en stor klinisk niche - udbredte, dårligt behandlede desmotivationsforstyrrelser. Tidligere "åbne" stimulanser imiterer ikke naturlig fysiologi. Derfor er det logisk at forsøge at lære implantatet at "tænke som mave-tarmkanalen": at registrere bolus og udløse fysiologisk peristaltik præcis der, hvor det naturlige signal passerer - ved plexus myentericus.
Et team fra MIT, Harvard og Brigham har skabt et miniature-øsofagus-/maveimplantat, der registrerer en fødevarebolus i et "lukket kredsløb" og udløser koordinerede bølger af peristaltik. Hos grise genoprettede enheden ikke kun spiserørs- og mavemotilitet, men inducerede også hormonelle ændringer svarende til den postprandiale (fodrede) tilstand. Implantatet placeres endoskopisk uden abdominal kirurgi. Undersøgelsen blev offentliggjort i tidsskriftet Nature.
Hvad fandt de på?
- Selve implantatet. En tynd "fibrøs" neuroprotese med en diameter på ≈1,25 mm med syv elektroder for hver 1 cm og en mikrokanal til lokal levering af stoffer (elektro- og kemostimulering). Dens fleksibilitet og dimensioner gør det muligt at indsætte den gennem en standard instrumentkanal på et endoskop (2,8-3,2 mm).
- Installation. Der er udviklet et endoskopisk instrument: en nål med et omvendt træk af en nitinol-"krog", hydrodissektion og det afgørende trick - at søge efter submucosa ved hjælp af vævsimpedans for præcis placering lige over muskellaget, nær den myenteriske plexus.
- Lukket kredsløb. Systemet aflæser bolussignalet (EMG/intraluminale sensorer) og vælger et stimuleringsmønster for at inducere sekventielle kontraktioner svarende til naturlig peristaltik. Det er muligt at kombinere "excitatoriske" og "inhiberende" stimuli, samt lokalt afslappe lukkemusklerne med mikrodoser af lægemidler.
Hvad blev vist på dyr
- Spiserør: Implantatet producerede "synkebølger" uden egentlig synkning, herunder kontrolleret afslapning af den nedre øsofagussfinkter (via mikroafgivelse af glukagon) og programmerbare fremadrettede/retrograde bølger - i bund og grund et peristaltisk "joystick".
- Mave. Efter 20 minutters stimulering steg peristaltikkens hyppighed cirka til det dobbelte sammenlignet med kontrolgruppen (n≈4, p<0,05).
- Metabolisk "illusion af mæthed". Ved faste førte 30-minutters stimulering (spiserør eller mave) til hormonelle ændringer: en stigning i GLP-1 og insulin, et fald i ghrelin (appetithormon); ved gastrisk stimulering blev der også observeret en stigning i glukagon. Profilen som helhed lignede den postprandiale tilstand.
Sikkerheds- og tekniske detaljer
Korte in vitro-biokompatibilitetstests (materialeekstrakter) viste ingen toksicitet; in vivo 7 dage efter implantation - normal vægstrækbarhed og ingen enhedens migration/grov vævsskade. (Yderligere holdbarhed og pålidelighed kræver langvarig testning.)
Hvorfor er dette nødvendigt?
- Dysmotilitet og refraktære tilstande. Achalasi, gastroparese, dysfagi, postoperative lidelser - hvor klassiske lægemidler/operationer ofte giver en ufuldstændig effekt. Lokal multikanalstimulering er tættere på reel fysiologi end eksisterende "single-channel" open-loop implantater.
- Metaboliske lidelser. Ved at kontrollere de afferente signalveje mellem tarm og hjerne kan enheden potentielt modulere appetit og stofskifte, hvilket er interessant for fedme/diabetes (hypotese indtil videre, intet bevis hos mennesker).
Begrænsninger og hvad der nu skal ske
Dette er præklinisk arbejde på grise i den akut-subakutte tilstand. Foran ligger langtidsstudier af kontaktstabilitet, energiforsyning, risiko for fibrose, præcise stimuleringsprotokoller og derefter tidlige kliniske forsøg på patienter med alvorlige former for dysmotorik. Men det er allerede blevet vist, at peristaltikken kan "tændes" på kommando, og hormonelle reaktioner kan ændres mod mæthedsfornemmelse - alt sammen gennem endoskopisk adgang.
