Nye publikationer
Ny tilgang blokerer kræftcellers tilpasning og fordobler effektiviteten af kemoterapi
Sidst revideret: 27.07.2025

Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
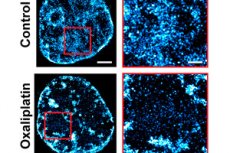
I en helt ny tilgang til kræftbehandling har biomedicinske ingeniører fra Northwestern University fordoblet effektiviteten af kemoterapi i et dyreforsøg.
I stedet for at angribe kræften direkte, forhindrer denne unikke strategi kræftceller i at udvikle sig til at blive resistente over for behandlinger – hvilket gør sygdommen mere modtagelig for eksisterende lægemidler. Denne tilgang udryddede ikke blot stort set sygdommen i cellekulturer, den forbedrede også effektiviteten af kemoterapi betydeligt i musemodeller af æggestokkræft.
Undersøgelsen blev offentliggjort i tidsskriftet Proceedings of the National Academy of Sciences.
"Kræftceller er fantastiske tilpasningsevner," siger Vadim Backman fra Northwestern University, som ledede studiet. "De kan tilpasse sig næsten alt. Først lærer de at undgå immunsystemet. Derefter lærer de at modstå kemoterapi, immunterapi og stråling. Når de bliver resistente over for disse behandlinger, lever de længere og får nye mutationer. Vi ønskede ikke at dræbe kræftcellerne direkte. Vi ønskede at tage deres superkraft væk - deres medfødte evne til at tilpasse sig, ændre sig og undgå."
Backman er Sachs Family Professor i biomedicinsk teknik og medicin på Northwestern Universitys McCormick School of Engineering, hvor han leder Center for Physical Genomics and Engineering. Han er også medlem af Robert H. Leury Comprehensive Cancer Center, Institute for the Chemistry of Life Processes og International Nanoscience Institute.
Kromatin er nøglen til kræftoverlevelse
Kræft har mange karakteristiske træk, men én egenskab ligger til grund for dem alle: dens ubarmhjertige evne til at overleve. Selv når immunsystemet og aggressive medicinske behandlinger angriber en tumor, kan kræften krympe eller aftage i vækst, men den forsvinder sjældent helt. Selvom genetiske mutationer bidrager til resistens, forekommer mutationerne for langsomt til at forklare kræftcellernes hurtige reaktion på stress.
I en række studier afdækkede Backmans team en fundamental mekanisme, der forklarer denne evne. Den komplekse organisering af genetisk materiale kaldet kromatin bestemmer kræfts evne til at tilpasse sig og overleve selv de kraftigste lægemidler.
Kromatin, en gruppe af makromolekyler, herunder DNA, RNA og proteiner, bestemmer hvilke gener der undertrykkes, og hvilke der udtrykkes. For at pakke de to meter DNA, der udgør genomet, ind i et rum på blot en hundrededel af en millimeter inde i cellekernen, er kromatin ekstremt komprimeret.
Ved at kombinere billeddannelse, modellering, systemanalyse og in vivo-eksperimenter fandt Backmans team ud af, at 3D-arkitekturen i denne pakke ikke kun styrer, hvilke gener der aktiveres, og hvordan celler reagerer på stress, men også tillader celler fysisk at kode en "hukommelse" af gentranskriptionsmønstre ind i selve pakkens geometri.
Genomets tredimensionelle arrangement fungerer som et selvlærende system, svarende til en maskinlæringsalgoritme. I takt med at det "lærer", omorganiseres dette arrangement konstant til tusindvis af nanoskopiske kromatin-pakningsdomæner. Hvert domæne lagrer et stykke af cellens transkriptionelle hukommelse, som bestemmer, hvordan cellen fungerer.
Omprogrammering af kromatin for at forbedre kemoterapi
I det nye studie udviklede Backman og hans kolleger en beregningsmodel, der bruger fysiske principper til at analysere, hvordan kromatinpakning påvirker en kræftcelles sandsynlighed for at overleve kemoterapi. Ved at anvende modellen på forskellige typer kræftceller og klasser af kemoterapimedicin fandt teamet, at det præcist kunne forudsige celleoverlevelse – selv før behandlingen begyndte.
Fordi kromatinpakning er afgørende for kræftcellers overlevelse, spurgte forskerne sig selv: hvad ville der ske, hvis pakningsarkitekturen blev ændret? I stedet for at skabe nye lægemidler screenede de hundredvis af eksisterende lægemidler for at finde kandidater, der kunne ændre det fysiske miljø inde i cellekerner og påvirke kromatinpakning.
I sidste ende valgte teamet celecoxib, et FDA-godkendt antiinflammatorisk lægemiddel, der allerede bruges til behandling af gigt og hjerte-kar-sygdomme, og som som en bivirkning ændrer pakningen af kromatin.
Eksperimentelle resultater
Ved at kombinere celecoxib med standardkemoterapi så forskerne en betydelig stigning i antallet af døde kræftceller.
I musemodeller af æggestokkræft reducerede en kombination af paclitaxel (et almindeligt kemoterapilægemiddel) og celecoxib hastigheden af kræftcelletilpasning og forbedrede tumorvækstundertrykkelsen, hvilket overgik effekten af paclitaxel alene.
"Da vi brugte en lav dosis kemoterapi, fortsatte tumorerne med at vokse. Men da vi først tilføjede en kandidat-TPR (transkriptionel plasticitetsregulator) til kemoterapien, så vi en langt mere signifikant væksthæmning. Det fordoblede effekten," sagde Backman.
Mulige udsigter
Denne strategi kan give læger mulighed for at bruge lavere doser kemoterapi, hvilket reducerer alvorlige bivirkninger. Dette ville forbedre patienternes komfort og deres oplevelse af kræftbehandling betydeligt.
Backman mener, at omprogrammering af kromatin kan være nøglen til behandling af andre komplekse sygdomme, herunder hjerte-kar-sygdomme og neurodegenerative sygdomme.
